新薬承認情報
2年前
【胃癌治療GL速報】ゾルベツキシマブを1次治療として推奨 : CLDN18.2陽性/HER2陰性進行胃癌

日本胃癌学会ガイドライン委員会は5月22日、 胃癌治療ガイドライン速報を公開し、 CLDN18.2陽性/HER2陰性で治癒切除不能な進行・再発胃癌の1次治療としての抗Claudin18.2抗体薬ゾルベツキシマブについて、 有効性および安全性を検証した2件の第III相二重盲検無作為化比較試験 (SPOTLIGHT、 GLOW) に関するコメントを発表した。
リンクはこちら
日本胃癌学会 胃癌治療ガイドライン速報
【速報】 CLDN18.2 陽性、 HER2 陰性の治癒切除不能な進行・再発胃癌/胃食道接合部癌に対する一次治療としての Zolbetuximab (ゾルベツキシマブ) のランダム化第 III 相試験 (SPOTLIGHT、 GLOW) に関する日本胃癌学会ガイドライン委員会のコメント
SPOTLIGHT試験
Lancet. 2023 May 20;401(10389):1655-1668. PMID: 37068504
GLOW試験
Nat Med. 2023 Aug;29(8):2133-2141. PMID: 37524953
日本人を含む両試験でPFS・OS改善
SPOTLIGHT試験およびGLOW試験の結果を受け、 同委員会は以下2点の観点から、 CLDN18.2陽性かつHER2陰性で治癒切除不能な進行・再発胃癌/胃食道接合部癌に対する1次治療として、 ゾルベツキシマブ+化学療法 (mFOLFOXまたはCAPOX) を推奨すると発表した。
① 両試験において、 化学療法単独に比べ、 ゾルベツキシマブ併用療法で有意な無増悪生存期間 (PFS) および全生存期間 (OS) の延長が示されたこと
② 両試験に日本人が含まれており、 国内症例に対するゾルベツキシマブ併用の安全性が確認されていること
初回投与から悪心・嘔吐対策が必須
またゾルベツキシマブは高い催吐性を持つため、 初回投与時から適切な制吐療法が必要とされる。同薬に伴う悪心・嘔吐の対応については、 日本癌治療学会による制吐薬適正使用ガイドライン速報を参照することとされた。
なお本速報は、 CLDN18.2陽性で治癒切除不能な進行・再発胃癌におけるゾルベツキシマブの国内承認 (3月) および薬価収載 (5月) を待ったうえで掲載されたという。 該当する新たな診断・治療法の推奨度はガイドラインが改訂されるまでの暫定として記載されている。
関連コンテンツ
関連レジメン
ゾルベツキシマブ+フルオロウラシル+レボホリナート+オキサリプラチン

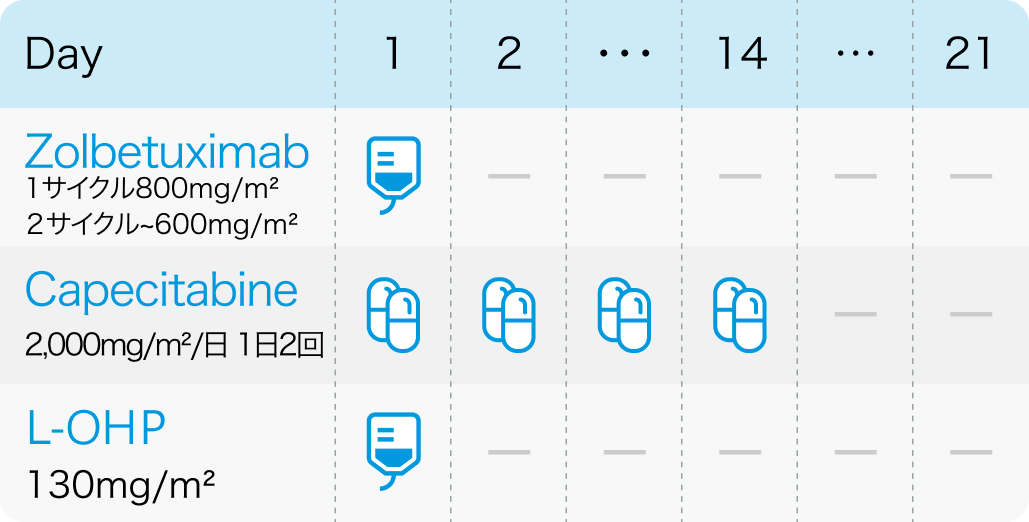
ゾルベツキシマブ+カペシタビン+オキサリプラチン
関連ポスト
解説 : 国立がん研究センター中央病院 山本駿先生
解説 : 国立がん研究センター東病院 中山厳馬先生
【速報】適正使用ガイド
【胃癌治療GL速報】ゾルベツキシマブを1次治療として推奨 : CLDN18.2陽性/HER2陰性進行胃癌の全コンテンツは、医師会員限定でアプリからご利用いただけます*。
*一部のコンテンツは非医師会員もご利用いただけます
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
QRコードから
アプリを
ダウンロード!