新薬承認情報
2年前
オシメルチニブとデュルバルマブ、 CRT後肺癌への単剤地固め療法で承認申請

アストラゼネカは7月31日、 第3世代EGFRチロシンキナーゼ阻害薬オシメルチニブおよび抗PD-L1抗体デュルバルマブの単剤療法について、 肺癌治療における根治的化学放射線療法 (CRT) 後の治療選択肢拡大に向けて承認申請を行ったと発表した。
オシメルチニブ申請はLAURA試験の結果に基づく
オシメルチニブは、 プラチナ製剤ベースのCRT後に病勢進行 (PD) を認めなかったEGFR変異を有する切除不能Ⅲ期非小細胞肺癌 (NSCLC) を対象に、 同薬による地固め療法の有効性について検証した第Ⅲ相二重盲検無作為化比較試験LAURAの結果に基づき、 6月末に承認申請が行われた。
同薬はプラセボと比較して病勢進行または死亡のリスクを84%低減させ (ハザード比 [HR] 0.16[95%CI 0.10-0.24]、 p<0.001)、 無増悪生存期間 (PFS) 中央値はオシメルチニブ群で39.1ヵ月、 プラセボ群で5.6ヵ月だった。 また。 事前に規定された全てのサブグループにおいて、 オシメルチニブ群のプラセボ群に対するPFS延長の優位性が一貫して認められた。
▼PFS率 (12ヵ月時、 24ヵ月時)
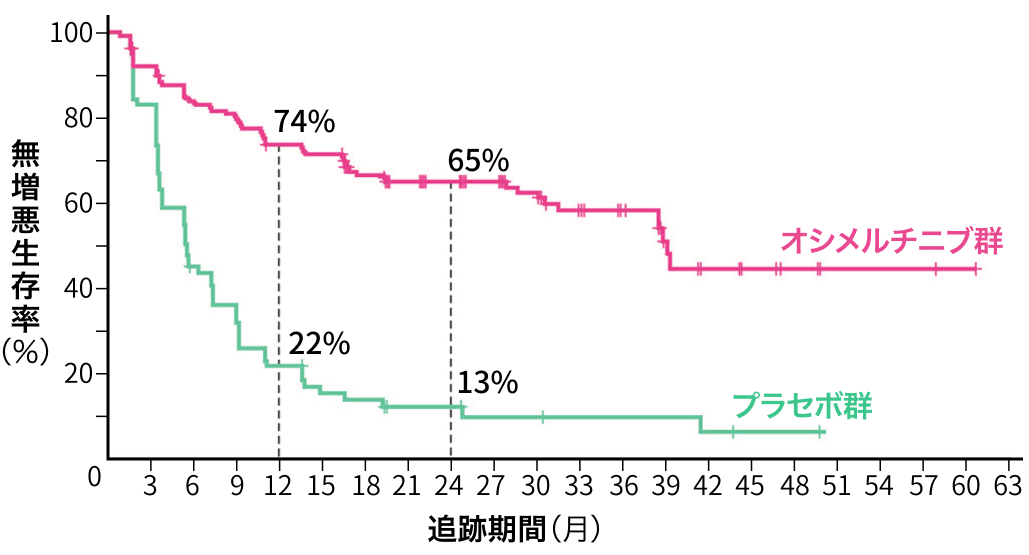
(N Engl J Med 2024年6月2日オンライン版)
>>LAURA試験の詳細はこちら
デュルバルマブ申請はADRIATIC試験の結果に基づく
デュルバルマブは、 プラチナ製剤をベースとしたCRT後にPDが認められなかった限局型小細胞肺癌 (LS-SCLC) に対する地固め療法としての同薬の有効性および安全性を評価した第Ⅲ相国際共同二重盲検無作為比較試験ADRIATICの初回中間解析の結果に基づき、 7月末に承認申請が行われた。
同薬はプラセボに対して死亡リスクを27%低下させ (全生存期間 [OS] のHR 0.73[95%CI 0.57-0.93]、 p=0.0104)、 主要評価項目であるOS中央値はデュルバルマブ群が55.9ヵ月、 プラセボ群が33.4ヵ月だった。 また、 デュルバルマブ群では病勢進行または死亡のリスクがプラセボと比較して24%低下し (PFSのHR 0.76[95%CI 0.61-0.95]、 p=0.0161)、 副次評価項目であるPFS中央値はデュルバルマブ群が16.6ヵ月、 プラセボ群で9.2ヵ月だった。
>>ADRIATIC試験の詳細はこちら
関連コンテンツ
関連ポスト

関連レジメン
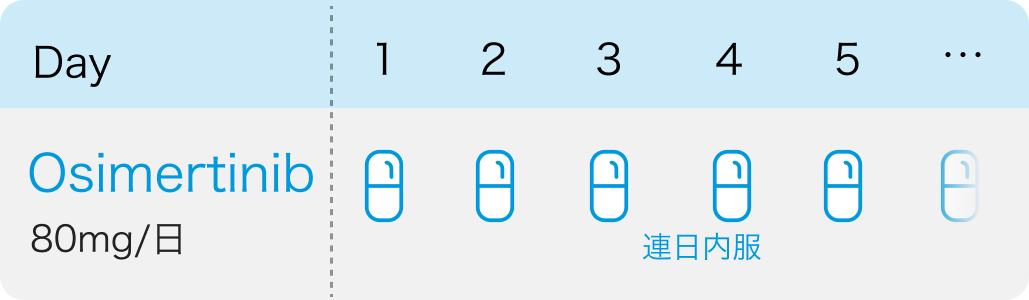
オシメルチニブ (タグリッソ®)
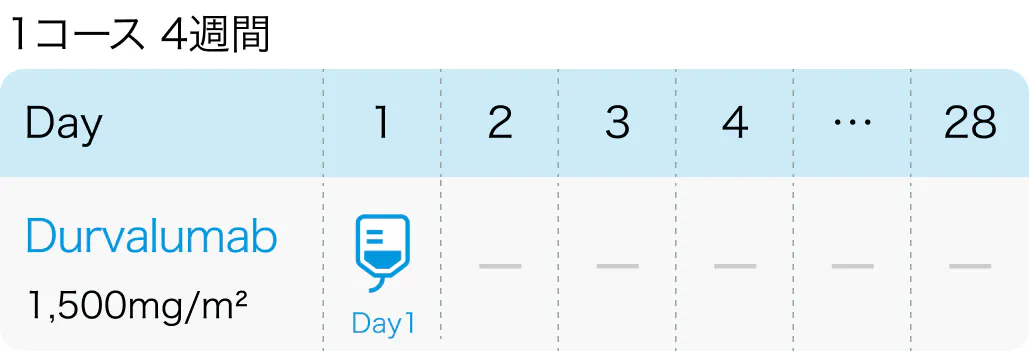
デュルバルマブ (イミフィンジ®)
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。