新薬承認情報
1年前
クアルソディ 「ALS」 等への適応追加-24年12月の承認情報まとめ-
25剤を承認、 うち新規有効成分14剤
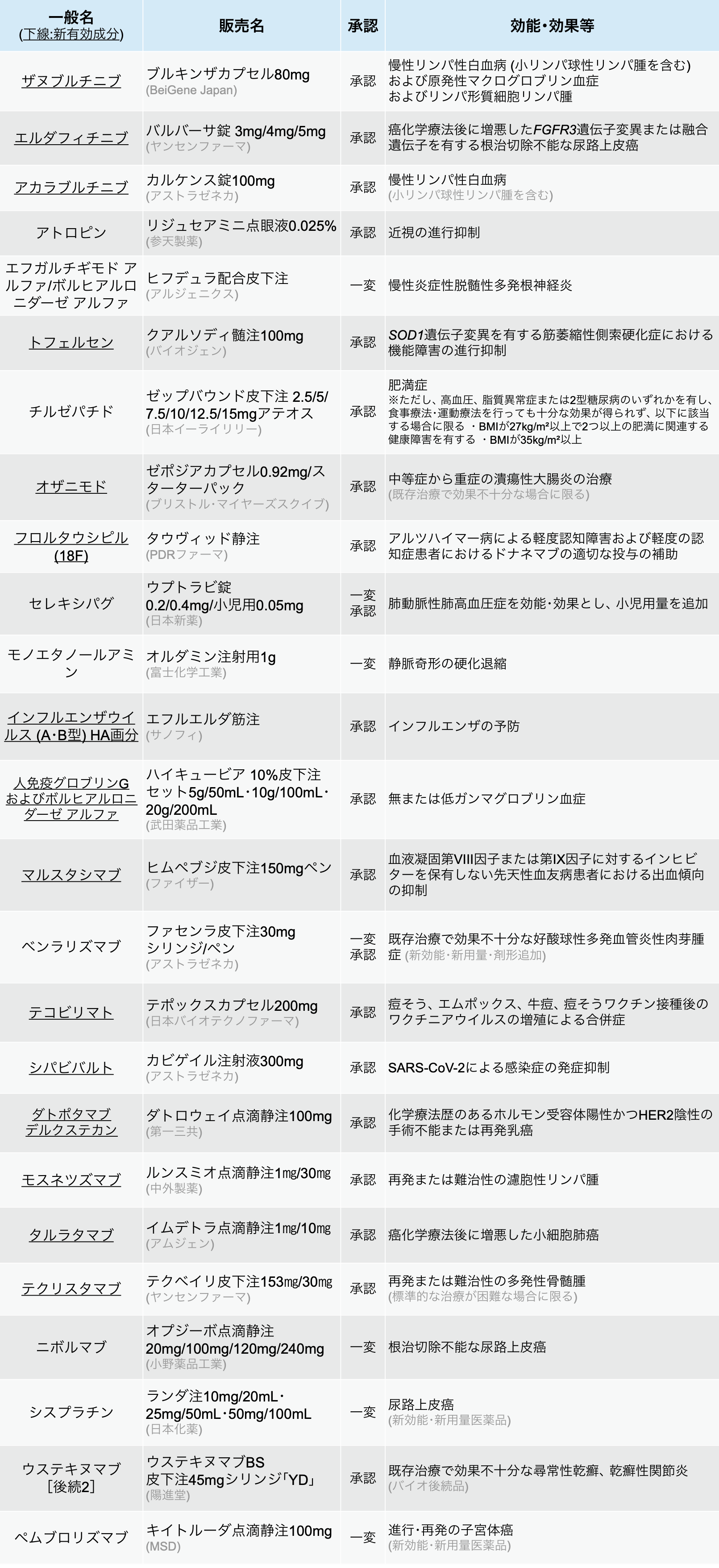
医薬品医療機器総合機構 (PMDA) は、 2024年12月に25種類の医薬品が厚生労働省から承認を受けたと発表した。 (うち新有効成分は14剤)
ヒフデュラ配合皮下注
ヒフデュラはエフガルチギモド アルファ (ウィフガート) の有効成分に浸透促進薬であるボルヒアルロニターゼ アルファを配合した皮下注製剤であり、 在宅での投与が可能。 全身型重症筋無力症、 慢性特発性血小板減少性紫斑病に続き、 慢性炎症性脱髄性多発根神経炎 (CIDP) が国内では3つ目の適応症となる。
今回の承認は、 未治療または免疫グロブリン療法もしくはコルチコステロイドの投与を受けているCIDP患者を対照に、 ヒフデュラの有効性および安全性を評価した、 国際共同二重盲検プラセボ対照無作為化比較試験ADHEREおよびその継続試験から得られた肯定的な結果に基づく。
トフェルセン
トフェルセン (商品名クアルソディ) はアンチセンスオリゴヌクレオチド (ASO) であり、 SOD1変異を有する筋萎縮性側索硬化症 (ALS) に対し、 遺伝的原因を標的とする治療薬として日本で初めて承認された。 SOD1変異は、 全世界のALS患者の約2%に認められる極めて希少な進行性疾患であるが、 日本ではSOD1変異例が最も多く、 約30%を占めるとされる。
今回の承認は、 SOD1変異陽性ALSを対象とした第Ⅲ相無作為化比較試験VALORおよび非盲検長期継続投与試験の結果に基づく。 VALOR試験において、 主要評価項目である投与28週時点のALSFRS-R合計スコアのベースラインからの変化量は統計学的有意差を示さなかったものの、 非盲検長期継続投与試験との併合解析では、 いずれの評価時点および解析対象集団においても、 トフェルセン群では対照群と比較して、 ALSFRS-R 合計スコアのベースラインからの変化量が小さい傾向を示した。
フロルタウシピル
フロルタウシピル¹⁸F (商品名タウヴィッド) は、 アルツハイマー病に関わるタンパク質 「タウ」 に結合する低分子化合物フロルタウシピルを放射性フッ素 (¹⁸F) で標識したPET検査用イメージング剤である。 今回、 アルツハイマー病による軽度認知障害および軽度認知症患者におけるドナネマブ (商品名ケサンラ) の適切な投与の補助として承認された。
(HOKUTO編集部の関連コンテンツに遷移します)
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。