新薬承認情報
1年前
ウステキヌマブ 「尋常性乾癬」 への適応追加-24年12月の承認情報まとめ-
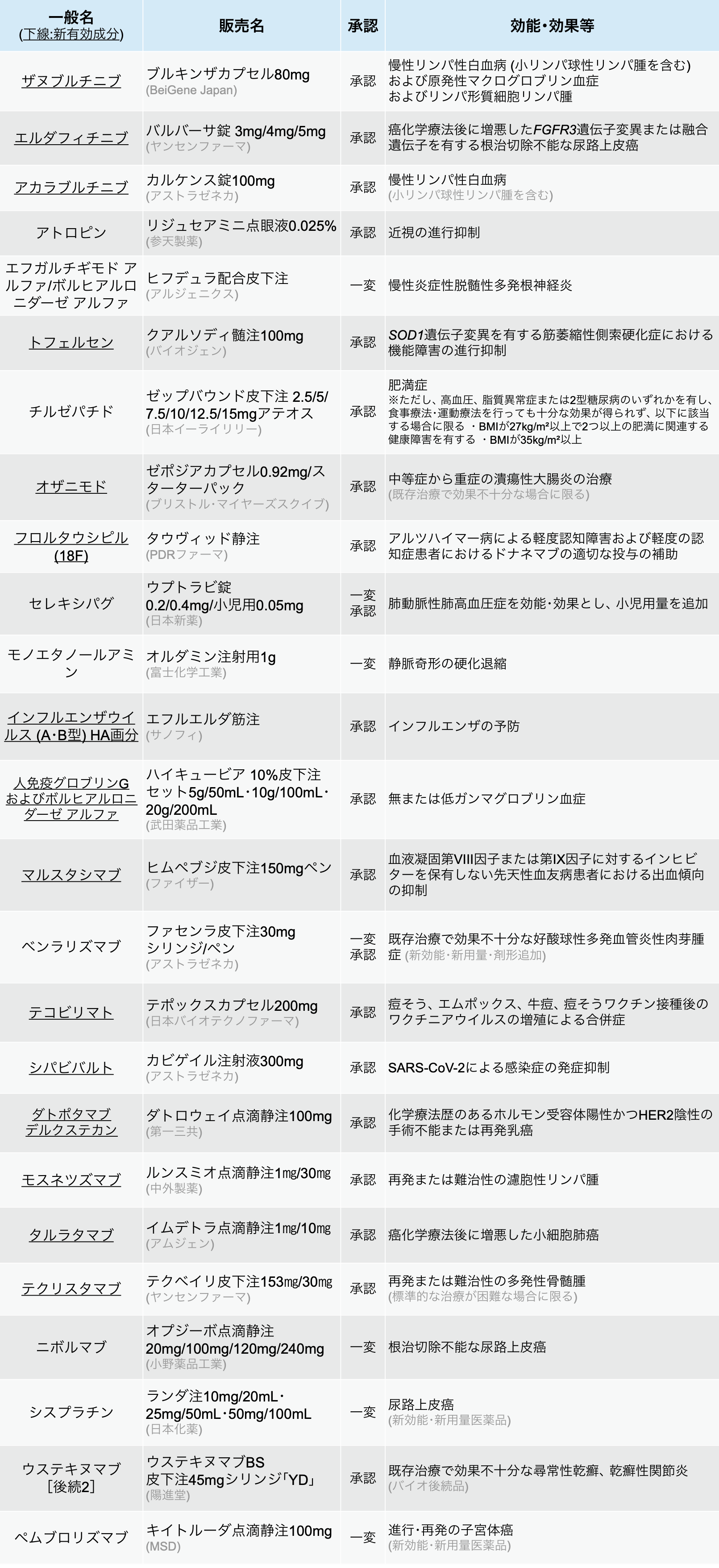
25剤を承認、 うち新規有効成分14剤
医薬品医療機器総合機構 (PMDA) は、 2024年12月に25種類の医薬品が厚生労働省から承認を受けたと発表した。 (うち新有効成分は14剤)
ウステキヌマブ
抗IL-12/23p40抗体ウステキヌマブ (商品名ステラーラ) のバイオ後続品であるウステキヌマブBS皮下注45mgシリンジ 「YD」 は今回、 紫外線療法を含む既存の全身療法 (生物学的製剤を除く) で効果不十分であり、 皮疹が体表面積の10%以上に及ぶ尋常性乾癬、乾癬性関節炎を効能・効果として、 一部変更承認された。
同薬の用法・用量は、 通常1回45mgを皮下投与する。 初回投与およびその4週後に投与し、 以降12週間隔で投与する。 ただし、 効果不十分な場合には1回90mgを投与することができる。
ウステキヌマブ 「尋常性乾癬」 への適応追加-24年12月の承認情報まとめ-の全コンテンツは、医師会員限定でアプリからご利用いただけます*。
*一部のコンテンツは非医師会員もご利用いただけます
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
QRコードから
アプリを
ダウンロード!