新薬承認情報
1年前
キイトルーダ 「子宮頸癌」 等への適応追加-11月の変更承認情報まとめ-
8剤を一部変更承認
医薬品医療機器総合機構 (PMDA) は、 2024年11月に8種類の医薬品が厚生労働省から承認を受けたと発表した。 (すべて一部変更承認)

ペムブロリズマブ
ペムブロリズマブ (商品名キイトルーダ®) は、 局所進行子宮頸癌に対するペムブロリズマブ+同時化学放射線療法 (CCRT) との併用が一部変更承認された。 CCRTとの併用療法において、 用法・用量は 「1回200mgを3週間間隔、 または1回400mgを6週間間隔で30分間かけて点滴静注し、 投与期間は24ヵ月間までとする」 とされている。
>> レジメンの詳細を見る
ペムブロリズマブ + 化学放射線治療
(外部サイトに遷移します)
デュルバルマブ
抗PD-L1抗体デュルバルマブ (商品名イミフィンジ®) は、 進行・再発子宮体癌に対し、 1次治療としてのデュルバルマブ+化学療法併用、 およびその後のデュルバルマブ単剤による維持療法として、 ミスマッチ修復機能 (MMR) の有無にかかわらず承認された。 また、 MMRが正常 (pMMR) な患者に対しては、 維持療法としてのデュルバルマブ+オラパリブ併用療法が併せて承認された。
今回の承認は、 新たに診断された進行または再発の上皮性子宮体癌699例を対象に行われた第Ⅲ相二重盲検プラセボ対照国際共同無作為化比較試験DUO-Eの結果に基づく。 デュルバルマブ投与群は、 MMR機能の有無にかかわらず、 プラセボ群と比較して病勢進行または死亡リスクが29%低減した (HR 0.71、 95%CI 0.57-0.89、 p=0.003)。 また、 デュルバルマブ+オラパリブ併用療法群は、 プラセボ群と比較し、 pMMR患者の病勢進行または死亡リスクを43%低減した (HR 0.57、 95%CI 0.44-0.73)。
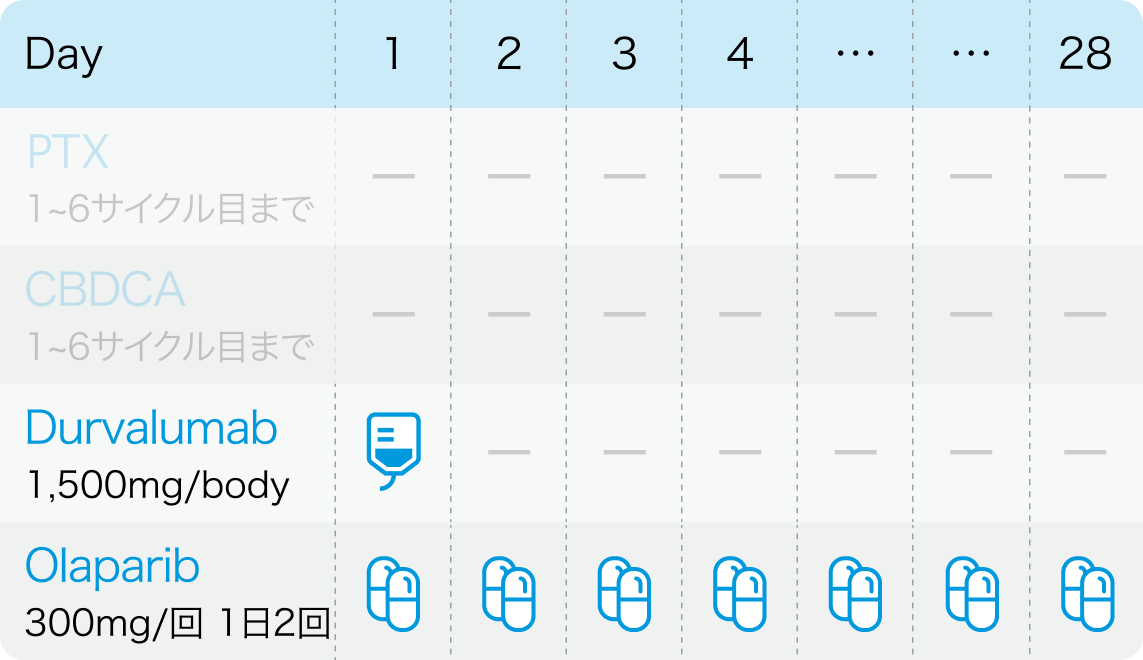
>> 関連レジメン : TC + Durvalumab ± Olaparib
子宮体癌(再発転移後 : 1次治療)

>> 最適使用推進ガイドライン
(外部サイトに遷移します)
オラパリブ
PARP阻害薬オラパリブ (商品名リムパーザ®) は、 pMMRの進行・再発子宮体癌における、 デュルバルマブを含む化学療法後の維持療法を効能・効果として承認された。 デュルバルマブと合わせ、 今回の承認は、 進行または再発子宮体癌を対象に、 1次治療としての化学療法+免疫チェックポイント阻害薬の併用、 および維持療法を目的としたICI+PARP阻害薬併用療法に対する初の承認となる。
>> 関連レジメン : TC + Durvalumab ± Olaparib
子宮体癌(再発転移後 : 1次治療)


>> 適正使用ガイド
(外部サイトに遷移します)
シスプラチン
シスプラチン (商品名ランダ®) は、 子宮頸癌に対するペムブロリズマブ+CCRT併用療法において一部変更承認された。 用法および用量は 「シスプラチンとして40mg/m² (体表面積) を1日1回投与し6日間休薬する。 これを1クールとして投与を繰り返す」。 なお、 投与量は患者の状態により適宜減量することとされている。
>> 関連レジメン:Pembrolizumab + CCRT
子宮頸癌 (初回治療)
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。