HOKUTO編集部
10ヶ月前
【消化器癌】2025年7月の注目論文3選 (山本駿先生)
食道癌や胃癌の治療では、 従来の殺細胞性抗癌薬に免疫チェックポイント阻害薬 (ICI) や分子標的薬を組み合わせた治療が、 周術期から転移・再発例まで幅広く臨床応用されている。
一方で、 高い臨床効果の背景にある作用機序の解明や、 後方治療のさらなる開発は依然として重要な課題である。 本稿では、 2025年7月までに報告された胃癌および食道癌に関する注目論文3件を取り上げ、 こうした課題に関する最新の知見を紹介する。

食道腺癌の周術期治療、 FLOTの遠隔再発はCRTよりも少ない
Recurrence Patterns of Esophageal Adenocarcinoma in the Phase III ESOPEC Trial Comparing Perioperative Chemotherapy With Preoperative Chemoradiotherapy
背景
ESOPEC試験は、 切除可能な局所進行食道腺癌を対象に、 CROSS試験で確立された術前化学放射線療法 (CRT) と、 術前後のFLOT療法 (5-FU、 レボホリナート、 オキサリプラチン、 ドセタキセル) を比較し、 FLOTの全生存期間 (OS) における優越性が検証された試験である。
一方、 CROSS試験の解析では局所再発は抑制されたものの、 遠隔再発への効果は限定的とされていた。 本研究では、 ESOPEC試験の追跡調査により、 両群の再発抑制効果が中心に比較検討された。
研究概要
本解析は、 第III相無作為化比較試験ESOPECに登録され、 腫瘍切除術を受けた438例を対象に実施された。 患者は、 術前後のFLOT療法+手術群と、 術前CRT (放射線41.4Gy+カルボプラチン+パクリタキセル) +手術群に1:1で無作為に割り付けられた。
FLOT群192例 (86.9%)、 CRT群179例 (82.5%) が手術を受け、 追跡期間中央値は56ヵ月であった。 評価項目は、 原因別死亡、 無再発生存期間 (RFS)、 再発部位とされた。
結果
主な結果は以下のとおり (FLOT群 vs CRT群)。
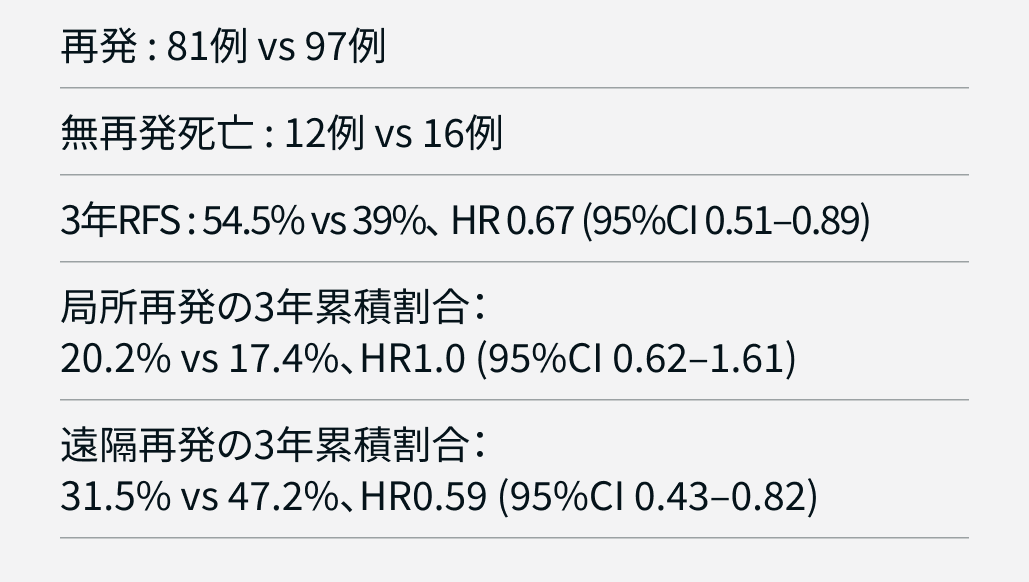
HR : ハザード比
CRTと比較して、 FLOT療法は局所再発抑制効果は同等だったが、 遠隔転移の抑制に優れ、 それが生存期間の延長に寄与したと考えられた。
My Opinion
ESOPEC試験は、 かつて本連載でも紹介した研究であり、 食道腺癌に対する現在の標準的な周術期治療である術前後のFLOT療法を確立したピボタル試験である。 今回の解析は、 FLOT療法の具体的な治療効果を再発様式などの観点から詳細に評価したものであり、 切除可能な局所進行病変の予後改善には、 局所制御だけでなく遠隔転移の抑制が不可欠であることが改めて示された。
本邦のJCOG1109試験では、 術前DCF (ドセタキセル+シスプラチン+フルオロウラシル) 療法群が術前CF (シスプラチン+フルオロウラシル) 療法群に対してOSの有意な延長を示した一方、 術前CF-RT群では同様の延長は確認されなかった。 今回のESOPEC試験結果と合わせて考えると、 切除可能病期の上部消化管癌では組織型を問わず、 遠隔転移の制御が予後改善の鍵となる。 TOPGEAR試験の知見も踏まえると、 今後の治療開発においては、 放射線療法よりも薬物療法の改良がより重要な課題といえる。 実際に、 MATTERHORN試験においてFLOT+デュルバルマブ併用療法の有効性が示されたことも、 この方向性を支持するものである。
すでに食道腺癌においては、 遺伝子発現に基づく個別化治療が周術期治療としても開発されつつあり、 食道扁平上皮癌では免疫チェックポイント阻害薬 (ICI) の併用を組み込んだ治療開発が進行中である。 その背景にある重要な戦略のひとつが、 今回の論文でも確認された遠隔転移の抑制であろう。
CLDN18.2標的ADCのP-I試験
CLDN18.2-targeting antibody-drug conjugate IBI343 in advanced gastric or gastroesophageal junction adenocarcinoma: a phase 1 trial
背景
胃癌および食道胃接合部癌 (G/GEJ癌) では、 CLDN18.2の高頻度発現が報告されており、 進行の早いこれらの癌種において有望な治療標的とされている。
既にCLDN18.2を標的としたモノクローナル抗体ゾルベツキシマブは、 SPOTLIGHT試験やGLOW試験の結果を踏まえ、 標準治療の1つとして位置付けられている。 一方、 抗体薬物複合体 (ADC) の開発も進められており、 完全ヒト化抗CLDN18.2抗体にエキサテカン誘導体を結合したADCであるIBI343の第I相試験が実施された。
研究概要
本試験では、 標準治療に不応または不耐の切除不能な進行・再発G/GEJ癌を対象に、 IBI343単剤療法の安全性と有効性が評価された。
試験は、 用量漸増パート (他の固形癌を含む) と、 CLDN18.2陽性例 (1+以上) に限定した用量拡張パートから構成され、 計127例が登録された (漸増パート19例、 拡張パート108例)。
結果
10mg/kg群では、 用量制限毒性が2例で確認され、 それぞれGrade 4の骨髄抑制、 およびGrade 4好中球減少+Grade 3発熱性好中球減少であった。 一部にGrade 3以上の消化器毒性がみられたが、 間質性肺炎の発現は認められなかった。
CLDN18.2高発現例 (2+/3+かつ75%以上) を対象とした6.0mg/kg群では、 奏効割合29%、 無増悪生存期間中央値5.5ヵ月であった。 薬物動態の結果も踏まえ、 推奨用量は6.0mg/kg (3週毎) と設定された。
IBI343は良好な忍容性と有望な有効性を示しており、 今後はHER2やPD-L1を標的とする複合治療、 ならびに治療シークエンスの最適化が期待される。
My Opinion
近年、 ADCの開発は急速に進展しており、 HER2陽性胃癌ではトラスツズマブ デルクステカンが既に標準治療として確立している。
本試験で評価されたIBI343は、 CLDN18.2を標的としたADCであり、 後方治療ラインにもかかわらず奏効割合約30%と有望な結果を示した。 用量拡張パートでは8.0mg/kg群も設定され、 CLDN18.2高発現例において奏効割合は47.1%とさらに高かったが、 病勢制御割合は6.0mg/kg群で90.3%、 8.0mg/kg群で88.2%と大差はなかった。
一方で、 有害事象の発現頻度は6.0mg/kg群と比較して8.0mg/kg群で高く、 Grade 3以上の白血球減少は19.4% vs 41.2%、 好中球減少は22.6% vs 47.1%であった。 薬物動態も考慮され、 推奨用量は6.0mg/kg (3週毎) と設定されたと考えられる。
なお、 IBI343と同様にCLDN18.2を標的としたADCとして、 CMG901/AZD0901やSHR-A1904もG/GEJ癌における有効性が報告されており、 今後のさらなる開発が期待される。
G/GEJ癌でのICI+化学療法、 相乗効果か相加効果か?
Investigating the Synergistic Effects of Pembrolizumab and Chemotherapy in Gastric and Gastroesophageal Junction Cancer
背景
ICIと細胞障害性抗癌薬の併用療法は、 KEYNOTE-859試験やCheckMate 649試験などにより、 HER2陰性の切除不能な進行・再発G/GEJ癌の標準治療として確立している。
一方で、 ICIと化学療法の併用において、 単なる上乗せ効果 (相加効果) にとどまらず相乗効果が存在するかどうかは明らかでなかった。 本研究では、 既存の臨床試験データを用いて、 ペムブロリズマブ+化学療法の相乗効果の有無を検討した。
研究概要
解析には、 ペムブロリズマブを含むKEYNOTE-061、 KEYNOTE-062、 KEYNOTE-859試験のKaplan–Meier曲線を用いてG/GEJ癌の症例データを再構築・抽出した。
各治療レジメンのPFS実測値と、 独立した薬剤作用モデルに基づいて推定したPFS予測値を比較した。 実測値が予測値を有意に上回る場合は相乗効果ありと判断した。
結果
PD-L1 CPS 1以上の2,194例におけるPFSは、 以下のとおりであった。

ペムブロリズマブと化学療法の併用療法におけるPFS実測値は、 各臨床試験のデータから推定されたPFS予測値と同程度であった。 したがって、 相乗効果は認められなかったものの、 両者の有効性を損なうことなく相加効果は確認された。
この結果は、 本併用療法が実臨床において引き続き有用な治療選択肢であることを支持すると考えられる。
My Opinion
以前より、 ICIと殺細胞性抗癌薬の併用療法においては、 殺細胞性抗癌薬が誘導するimmunogenic cell deathにより、 ICIの効果が増強される可能性が示唆されてきた。 今回の解析では、 ICI併用による相乗効果の有無を検討したが、 明らかな相乗効果は認められなかった。 一方で、 互いの治療効果を減弱させる所見は認められず、 相加効果は示されたことから、 今後の薬剤開発において有用な知見となるだろう。
現在、 進行G/GEJ癌においては、 TIGITを標的としたICI、 FGFR2bを標的とする分子標的薬、 CLDN18.2を標的としたADCや細胞療法の開発が進められている。 また、 食道扁平上皮癌においても、 FGFRやTROP-2、 B7-H3を標的とした新規薬剤の臨床開発が進行中であり、 これらを既存の標準治療に組み合わせることで得られる相乗効果の有無についても、 今後の検討が期待される。
出典
HOKUTO関連コンテンツ
▼ASCO2025、 消化器癌関連記事
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。