HOKUTO編集部
1年前
乳癌へのPARP阻害薬、 オラパリブとタラゾパリブの使いどころは? (下村昭彦氏)

PARP阻害薬 (オラパリブ、 タラゾパリブ) は、 BRCA変異陽性乳癌に対する有効な治療選択肢として注目されている。 オラパリブおよびタラゾパリブの有効性と使い分けについて、 国立国際医療研究センター病院・がん総合内科/乳腺・腫瘍内科医長の下村昭彦氏が第62回日本癌治療学会 (JSCO 2024) で発表した。
転移乳癌におけるPARP阻害薬
まず下村氏は、 転移乳癌に対するPARP阻害薬として現在日本で使用可能であるオラパリブ、 タラゾパリブについて、 各薬剤のエビデンスを解説した。
オラパリブ : OlympiAD試験
オラパリブの有効性は、 第Ⅲ相試験OlympiADにおいて示されている。 同試験では、 生殖細胞系列BRCA1/2変異を有するHER2陰性の転移乳癌へのオラパリブの有効性について、 担当医選択の化学療法を対照に検証され、 無増悪生存期間 (PFS) の有意な改善が示された(中央値 7.0ヵ月 vs 4.2ヵ月、 HR 0.58 [95%CI 0.43-0.80]、 p<0.001)。
一方、 全生存期間 (OS) は両群で有意差を認めなかった(中央値19.3ヵ月 vs 17.1ヵ月、 HR 0.90 [同 0.66-1.23]、 p=0.513)。 ただし、 探索的解析では、 転移病変に対する化学療法歴のない患者集団においてはOSが良好な傾向を認めた (中央値22.6ヵ月 vs 14.7ヵ月、 HR 0.51 [同 0.29-0.90]、 p=0.02)。
N Engl J Med. 2017; 377: 523-533.
Ann Oncol. 2019; 30: 558-566.
タラゾパリブ : EMBRACA試験
タラゾパリブの有効性は、 第Ⅲ相試験EMBRACAにおいて示されている。 EMBRACA試験では、 BRCA1/2変異を有するHER2陰性局所進行または転移乳癌を対象に、 タラゾパリブの有効性について担当医選択の化学療法を対照に検証し、 PFSの有意な改善が示された (中央値 8.6ヵ月 vs 5.6ヵ月、HR 0.54 [95%CI 0.41-0.71]、 p<0.001)。
サブグループ解析では、 ホルモン受容体陽性例でより良好な成績が認められた(HR 0.47[同 0.32-0.70] )。 一方で、 OSはオラパリブと同様、 両群で有意差を認めなかった (中央値 19.3ヵ月 vs 19.5ヵ月、 HR 0.848 [同 0.670-1.073]、 p=0.17)。
N Engl J Med. 2018;379(8):753-763.
周術期治療におけるPARP阻害薬
次に下村氏は、 早期乳癌に対する術後治療として現在国内で使用可能であるオラパリブのエビデンスを解説した。
オラパリブ : OlympiA試験

術後オラパリブの有効性は第Ⅲ相試験OlympiAにおいて示されている。 OlympiA試験では、 局所治療および標準的な術前または術後化学療法を完了した生殖細胞系列BRCA変異陽性・HER2陰性の再発高リスク早期乳癌に対する術後療法としてのオラパリブの有効性について、 プラセボを対照に検証した。
患者背景は、 両群ともトリプルネガティブ乳癌 (TNBC) が80%以上、 閉経前が60%以上であった。 化学療法は約半数が術後、 残りの半数が術前に実施されていた。 90%以上が、 アントラサイクリン+タキサン製剤の療法を含むレジメンを受けていた。
オラパリブ群は主要評価項目である無浸潤疾患生存期間 (IDFS) の有意な改善を示し (3年IDFS率 85.9% vs 77.1%、 HR 0.58[99.5%CI 0.41-0.82]、 p<0.0001)、 副次評価項目である遠隔無病生存期間 (DDFS) も改善を示した (3年DDFS率 87.5% vs 80.4%、 HR 0.57 [同 0.39-0.83]、 p<0.0001)。 さらに2回目のOS中間解析の結果、 全集団のOSも有意に改善を示した (HR 0.68 [98.5%CI 0.47-0.97]、 p=0.009)。 以上の結果から、 術後療法としてのオラパリブは標準治療の1つとなっている。
▼オラパリブ/タラゾパリブの標的と期待される効果一覧
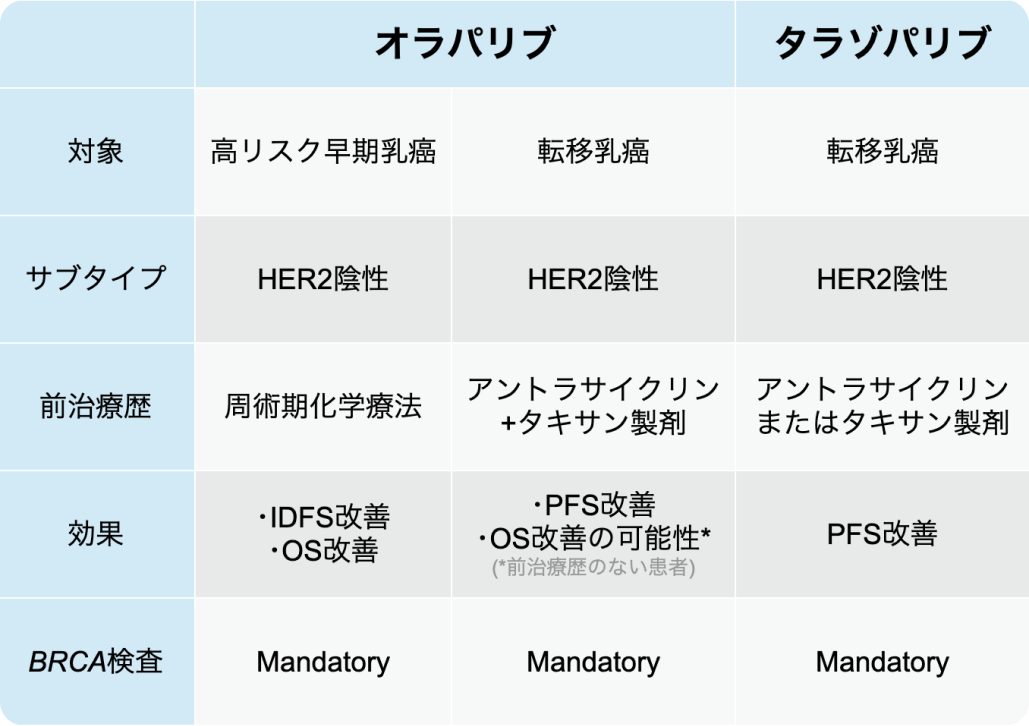
(下村氏講演資料を基に編集部作成)
2剤をどう使い分ける?
以上より下村氏は、 現在の日本において、 乳癌に対するオラパリブとタラゾパリブの使い分けや再投与の考え方について説明した。
使い分けに明確な基準はない
転移乳癌に対してはオラパリブとタラゾパリブのどちらも使用可能であり、 両剤ともPFSを改善する一方、 OSの改善は示されていない。 また毒性も両薬剤でほぼ同等の結果であった。
OlympiAD試験、 EMBRACA試験のサブグループ (ホルモン受容体陽性or陰性など) における結果はやや異なるものの、 その後オラパリブ単剤療法の有効性をリアルワールドで確認したLUCY試験ではホルモン受容体陽性例でやや生存率が高い傾向となり、 サブグループをもとにした実臨床での2剤の明確な使い分けは難しいのが現状だという。
次治療への移行困難なPD例には再投与・スイッチを検討
では、 2剤が使用できるのであれば、 再投与 (リチャレンジ) やスイッチは可能なのか。
このような臨床疑問に関して、 下村氏は、 「プラチナ製剤に感受性のある卵巣癌患者では、 オラパリブのリチャレンジの有効性が認められている」 と指摘した。 一方、 乳癌では、 プラチナ投与歴がある場合にむしろPARP阻害薬の有効性が劣り、 卵巣癌での結果を乳癌に応用することは難しいという。
さらに、 PARP阻害薬に対する耐性の約7割が機能回復変異 (リバージョン) であり、 基本的に再投与の有効性は低いと考えられている。 これに関して、 下村氏は 「ただし全ての患者でリバージョンが起こるわけではないため、 病勢進行 (PD) で次治療に移行することが可能な症例では試しても良いかもしれない」 と補足した。
乳癌コンパニオン診断としてのBRCA遺伝学的検査
PARP阻害薬は、 乳癌診療においてBRCA変異陽性という新たなサブタイプを認識させた。 一方で、 PARP阻害薬の使用においては、 コンパニオン診断としてのBRCA遺伝学的検査が必要となった。 これが 「新たな問題」 になっているという。
ホルモン受容体陽性でも、 適応対象には積極的にコンパニオン診断を
NCCNガイドラインでは、 PARP阻害薬に適応のある患者には全例に同薬を使用することが推奨されており¹⁾、 適応の有無をコンパニオン診断で評価することが重要となる。 このように、 コンパニオン診断による遺伝学的検査の重要性が認識される一方で、 ホルモン受容体陽性患者ではTNBC患者と比べてBRCA変異を有する割合が低いため、 臨床現場では遺伝学的検査の必要性を低く認識している医師がいるという。
しかしホルモン受容体陽性患者の絶対数がTNBCに比べて多いため、 実数で考えた場合、 BRCA変異陽性例の多くはホルモン受容体陽性患者に認められるという。 下村氏は 「従って、 ホルモン受容体陽性であっても対象となる症例にはコンパニオン診断を行うことが重要である」 と述べた。
なお『乳癌診療ガイドライン2022年版』(編 : 日本乳癌学会) では、 再発リスクにかかわらず、 遺伝性乳癌卵巣癌 (HBOC) のサーベイランスを行うことが推奨されている。
本邦では、 BRCA遺伝学的検査は
①45歳以下の発症
②60歳以下発症かつサブタイプがTNBC
③両側or片側に2個以上の原発乳癌を有する
④男性乳癌
⑤診断時に卵巣癌・卵管癌・腹膜癌のいずれかを合併している
⑥血縁者 (第3度近親者内) に乳癌・卵巣癌・膵癌患者の家族歴を有する
――のいずれかに当てはまる場合に保険適用となっている²⁾。 またASCO/SSOガイドラインでは、 65歳以下の患者には全員、 66歳以上には症例に応じてコンパニオン診断を実施することが推奨されている³⁾。
最後に、 同氏は 「乳癌診療におけるBRCA遺伝子検査の目的は、 HBOCの診断、 およびPARP阻害薬の適応に関するコンパニオン診断の2つが挙げられる。 多くの患者では遺伝学的検査が両方の目的を持つため、 患者も医療者も遺伝学的検査の目的を混乱することが多いが、 HBOC診断という目的がなくても、 コンパニオン診断の対象となる患者には積極的に検査を行うことが望ましい」 と説明した。
関連コンテンツ
Olaparib
Talazoparib
出典
¹⁾ NCCN Guidelines Version 2.2025
²⁾ 乳癌診療ガイドライン2022年版
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。