HOKUTO編集部
2年前
【肝細胞癌】Atzo+BevとDur+Trem、 どの症例に何を使う?

進行再発肝細胞癌の初回治療として、 2020年に抗PD-L1抗体であるアテゾリズマブとベバシズマブの併用療法 (Atzo+Bev) が承認され、 肝細胞癌の治療に免疫チェックポイント阻害薬 (ICI) が登場した。 その後、 2023年にはデュルバルマブ+トレメリムマブ (Dur+Trem) が治療選択肢に加わり、 ICIが治療の中心となってきている。
「肝癌診療ガイドライン 2021年版」では、 Atzo+BevとDur+Tremは進行肝細胞癌の1次治療に並列で記載されており、 両レジメンの使い分けは明確となっていない。 本稿ではAtzo+BevとDur+Tremに関して解説を行う。
著者 : 丸木雄太先生
国立がん研究センター中央病院 肝胆膵内科、 がんゲノム情報管理センター (C-CAT) 情報利活用戦略室 (併任)
Atzo+Bev
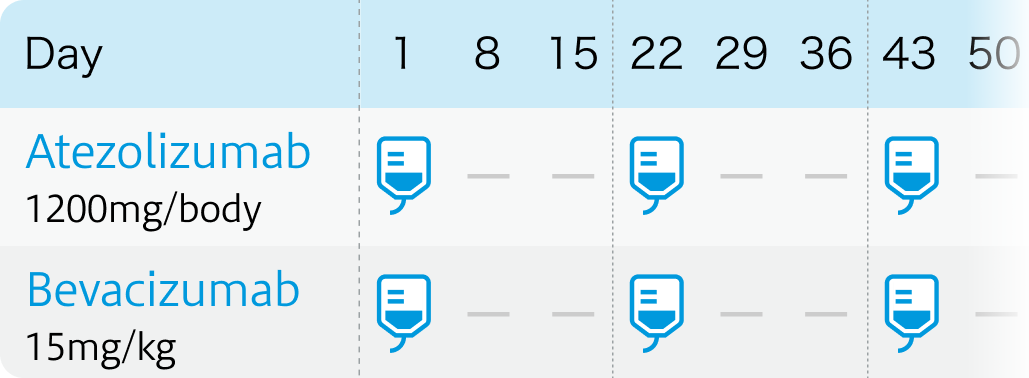
1サイクル3週間で、 アテゾリズマブ1200mg/bodyとベバシズマブ15mg/kgをDay1に繰り返し投与する
IMbrave150試験¹⁾は進行肝細胞がん患者を対象とし、 ソラフェニブとAtzo+Bevを比較する第III相国際共同試験であり、 Atzo+Bevがソラフェニブに対して全生存期間および無増悪生存期間の有意な延長を認めた。
▼有効性
主要評価項目であるOS中央値は、 Atzo+Bev群で19.2ヵ月、 ソラフェニブ群で13.4ヵ月であり、 層別ハザード比は0.66 (95%CI 0.52-0.85、 p<0.001) であった。 客観的奏効割合はAtzo+Bev群で30% (95%CI 25-35) に対してソラフェニブ群で11% (95%CI 7-17) であった。
▼安全性
全Gradeの有害事象はAtzo+Bev群で98%、 ソラフェニブ群で99%に発生し、 Grade 3以上の有害事象は各群でそれぞれ63%、 57%で発生した。
主な治療関連の有害事象は、 Atzo+Bev群でタンパク尿29%、 高血圧28%、 アスパラギン酸アミノトランスフェラーゼ増加16%、 疲労16%であった。 ソラフェニブ群では、 手足症候群48%、 下痢44%であった。
ICIの使用により発生する免疫介在性有害事象 (imAE) において、最も多かったものは肝炎であり、 全GradeでAtzo+Bev投与により53%認められた。
Atzo+Bevは、 これまでの肝細胞癌治療において不足していた腫瘍縮小が期待できる治療である。 本治療をきっかけに、 肝細胞癌に対するICI治療の可能性が開けたと言える。
Dur+Trem (STRIDEレジメン)
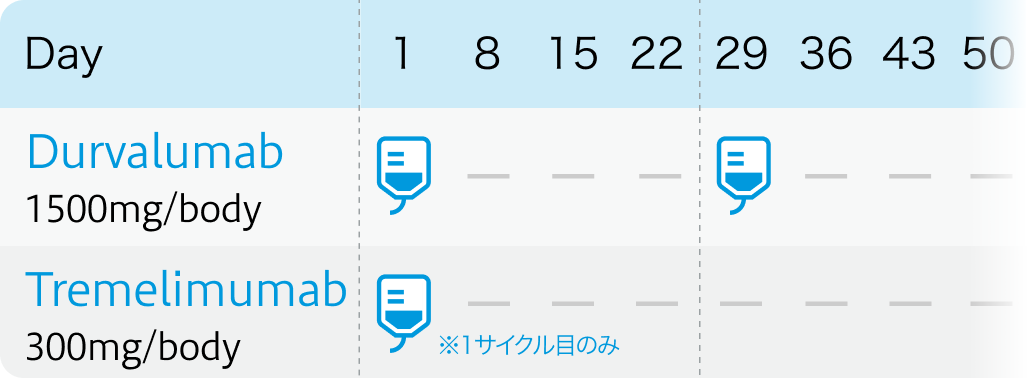
1サイクル4週間で、 デュルバルマブ1500mg/bodyとベバシズマブ300mg/bodyを1サイクル目のDay1に、 2サイクル目以降はデュルバルマブ1500mg/bodyをDay1に繰り返し投与する
HIMALAYA試験²⁾では、 デュルバルマブ (抗PD-L1抗体) に、 免疫反応を誘導する高用量のトレメリムマブ (抗CTLA4抗体) 単回投与を追加した併用療法(Dur+Trem; STRIDE*レジメン) により、 ソラフェニブと比較してOSの有意な延長が示された。
*Single Tremelimumab Regular Interval Durvalumab
▼有効性
主要評価項目であるOS中央値はDur+Trem群で16.4ヵ月、 ソラフェニブ群で113.7ヵ月であり、 層別ハザード比は0.78 (95%CI 0.65-0.93) であった。
▼安全性
全Gradeの有害事象はDur+Trem群で97%、 ソラフェニブ群で95%に発生し、 Grade 3以上の有害事象は各群でそれぞれ50%、 52%で発生した。
主な治療関連の有害事象は、 Dur+Trem群で下痢26%、 掻痒感23%であった。 ソラフェニブ群では、 手足症候群46%、 下痢44%であった。
imAEはDur+Trem群で35%に報告され、 その中でステロイドを必要としたのは20%であった。
Dur+Tremは肝細胞癌の薬物療法で、 VEGF阻害薬が使用されない初めての治療法である。 本治療の承認により、 これまでは治療導入が躊躇された、 胃食道静脈瘤による消化管出血リスクの高い患者への治療選択を広げることが可能となった。
一方、 複合免疫療法であることから、 これまでのAtzo+Bev療法よりもimAEの頻度が高くなっており、 治療中のimAEに対するマネジメントが重要である。
Atzo+BevとDur+Tremの使い分け :
4つの視点
❶患者背景
Atzo+BevはVGFR阻害作用のあるベバシズマブが含まれることから、 出血リスクや血栓形成リスクがある患者では使用しにくい傾向にある。
肝細胞癌患者は、 背景に肝硬変を有することが大半であり、 門脈圧亢進の状況では、 胃食道静脈瘤を合併している患者も見られる。 このような患者に対しては、 胃食道静脈瘤の治療と同時のAtzo+Bevは避ける必要があるためDur+Tremが優先される。
また、 糖尿病合併例や、 レンバチニブをはじめとしたチロシンキナーゼ阻害薬 (TKI) が局所治療と併用された経験がある症例、 抗癌薬開始前から蛋白尿を認める症例、 高血圧のコントロールが不十分な症例では、 ベバシズマブの使用が躊躇され、 Dur+Tremが優先されると考えられる。
❷適格基準
進行肝細胞癌では、 脈管侵襲を伴う症例がある。 肝細胞癌を対象とした第III相試験では、 門脈本幹に腫瘍栓が及ぶVp4の症例が除外される傾向にある。
しかし、 IMbrave150試験はVp4症例も適格とされている。 このことから、 Vp4症例では、 エビデンスのあるAtzo+Bevが優先されるべきと考える。
❸有害事象
Dur+Tremでは、 imAEの頻度が多く報告されている。 重症なimAEでは、 生命の危機が隣り合わせとなることもある。
そのため、 Dur+Tremはある程度のimAEに耐えうる患者が適格と考える。 具体的には、 ADLが保たれており、 副作用に対するセルフマネジメントが可能な患者といえる。
重要臓器機能の低下を合併している患者や認知機能の低下した高齢患者にDur+Trem療法を行う際は、 十分な注意が必要である。
❹長期予後
進行肝細胞癌患者にとって、 重要な治療目標は長期生存と考えられる。 先日行われた欧州臨床腫瘍学会(ESMO 2024)において、 HIMALAYA試験の5年フォローアップデータが示され、 Dur+Trem群で5年OS率が19.6%と報告された³⁾。
OS率
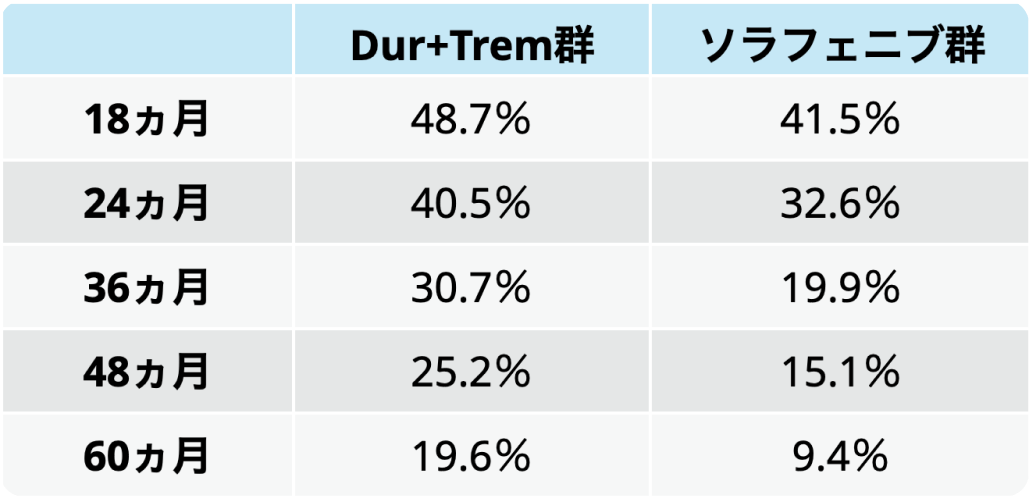
進行肝細胞癌において、 5人に1人が5年間の生存が得られる可能性のある治療といえる。 本結果から、 長期生存を狙う選択肢としてDur+Tremが挙げられる。
進行肝細胞癌に対する1次治療は、 ICIの登場により治療方針が大きく変化している。 今後も複数のICIを含むレジメンの承認が検討されていることから、 治療薬の特徴と患者個人の状態をしっかり把握して治療選択を行うことが求められる。
<出典>
1) N Engl J Med. 2020 May 14; 382(20): 1894-1905.
2) NEJM Evid. 2022 Aug; 1(8): EVIDoa2100070.
3) Ann Oncol. 2024. Sep; 35(Suppl 2): S656.
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。