新薬承認情報
1年前
【新発売】トラロキヌマブ ペン剤 (アドトラーザ®皮下注300mgペン)~アトピー性皮膚炎に対して~

抗IL-13抗体トラロキヌマブのオートインジェクター製剤である 「アドトラーザ®皮下注300mgペン」 が、 既存治療で効果不十分なアトピー性皮膚炎に対して2024年7月に承認、 11月20日に薬価収載、 12月2日に発売された。
より簡便な操作での投与が可能に
既存のプレフィルドシリンジ製剤である 「アドトラーザ®皮下注150mgシリンジ」 は、 2022年12月に承認され、 2024年4月から 「在宅自己注射」 が保険適用されている。
今回発売されたアドトラーザ®300mgペン製剤は、 より簡便な注射操作による治療を提供するためのもので、 患者の身体的な負担軽減および利便性の向上が期待されている。
薬剤情報
抗IL-13抗体トラロキヌマブ
*レオファーマ株式会社の外部サイトへ遷移します
効能または効果
既存治療で効果不十分なアトピー性皮膚炎
薬価
300mg 2mL1キット 4万1,859円
用法・用量
通常、 成人にはトラロキヌマブ (遺伝子組換え) として初回に600mgを皮下投与し、 その後は1回300mgを2週間隔で皮下投与する。
用法および用量に関連する注意
本剤による治療反応は、 通常投与開始から16週までには得られる。 16週までに治療反応が得られない場合は、 投与中止を考慮すること。
関連する臨床試験
成人対象の国際第III相試験 (単剤)
Br J Dermatol. 2021 Mar;184(3):437-49.
成人対象の国際第III相試験 (外用剤併用)
Br J Dermatol. 2021 Mar;184(3):450-63.
関連コンテンツ
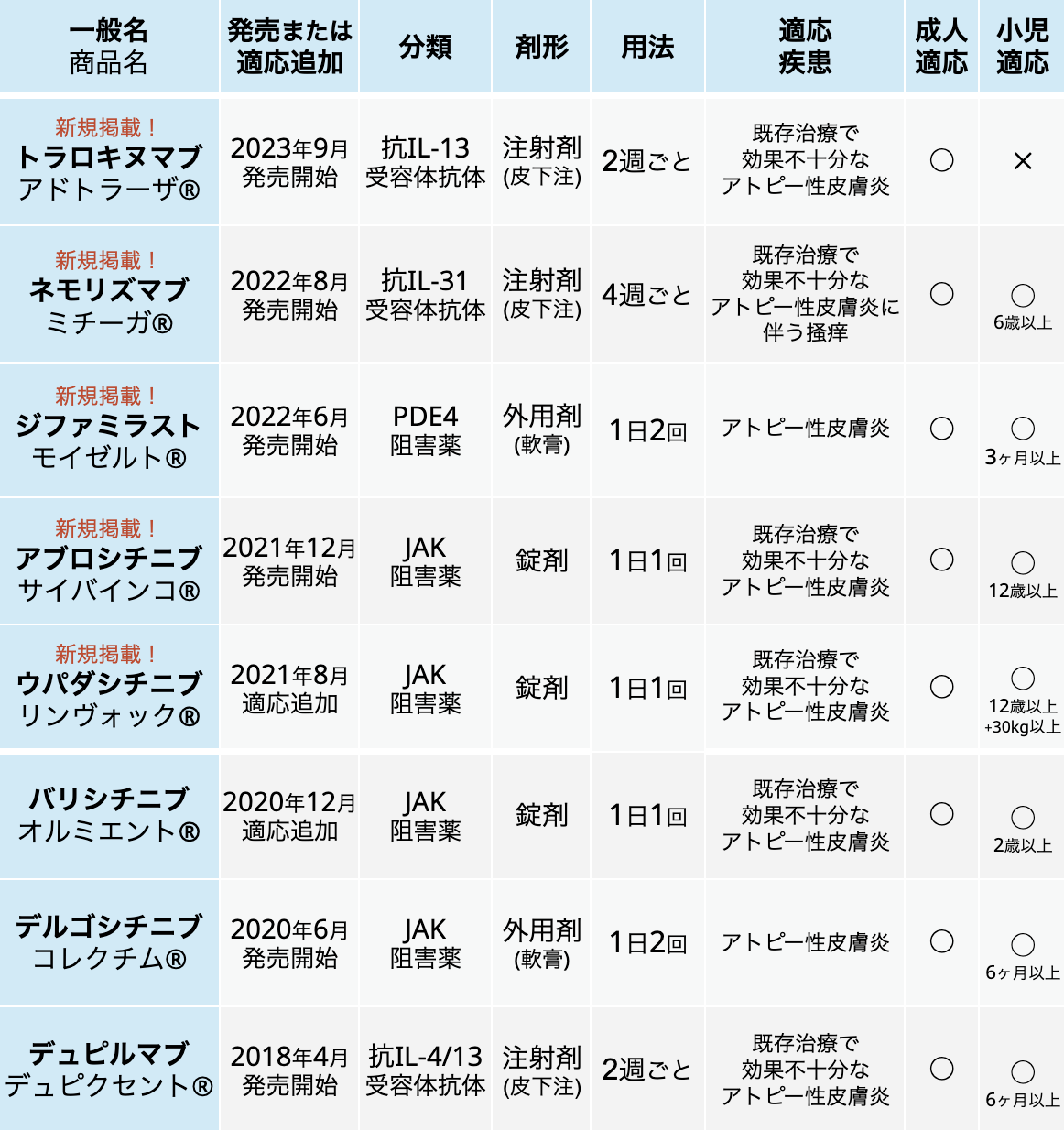
アトピー性皮膚炎診療GL2024の生物学的製剤まとめ
ヒト型抗IL−13受容体モノクローナル抗体
【新発売】トラロキヌマブ ペン剤 (アドトラーザ®皮下注300mgペン)~アトピー性皮膚炎に対して~の全コンテンツは、医師会員限定でアプリからご利用いただけます*。
*一部のコンテンツは非医師会員もご利用いただけます
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
QRコードから
アプリを
ダウンロード!