新薬承認情報
1年前
バルバーサ 「尿路上皮癌」 等への適応追加-24年12月の承認情報まとめ-
25剤を承認、 うち新規有効成分14剤
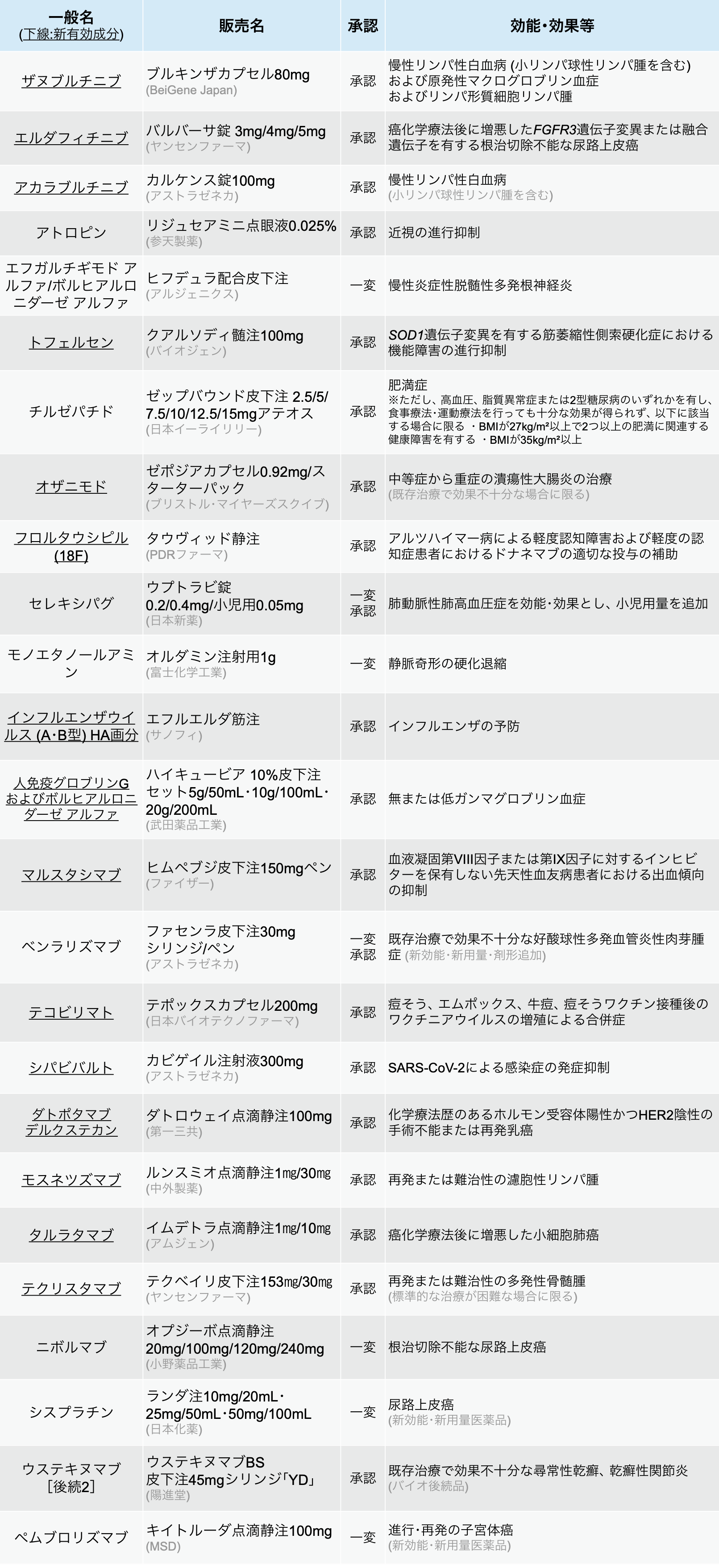
医薬品医療機器総合機構 (PMDA) は、 2024年12月に25種類の医薬品が厚生労働省から承認を受けたと発表した。 (うち新有効成分は14剤)
エルダフィチニブ
エルダフィチニブ (商品名バルバーサ) は1日1回経口投与のFGFRチロシンキナーゼ阻害薬であり、 癌化学療法後に増悪したFGFR3遺伝子変異または融合遺伝子を有する根治切除不能な尿路上皮癌を効能・効果として承認された。
今回の承認は、 日本および海外で実施された第III相非盲検無作為化比較試験THORの結果に基づく。 主要評価項目である全生存期間 (OS) 中央値は、 標準化学療法群に比べ、 エルダフィチニブ群で有意な改善を示した (12.1ヵ月vs7.8ヵ月、 HR 0.64[95%CI 0.47-0.88]、 p=0.005)。
また、 エルダフィチニブは今回、 FGFR3遺伝子変異または融合遺伝子を有する尿路上皮癌のコンパニオン診断としても同時承認されている。
>> 関連レジメン
(HOKUTO編集部の関連コンテンツに遷移します)
ニボルマブ
ニボルマブ (商品名オプジーボ) は2022年3月、 単剤療法で、 尿路上皮癌における術後補助療法を効能・効果として承認されている。 今回は尿路上皮癌に対する1次治療としての効能・効果で承認された。
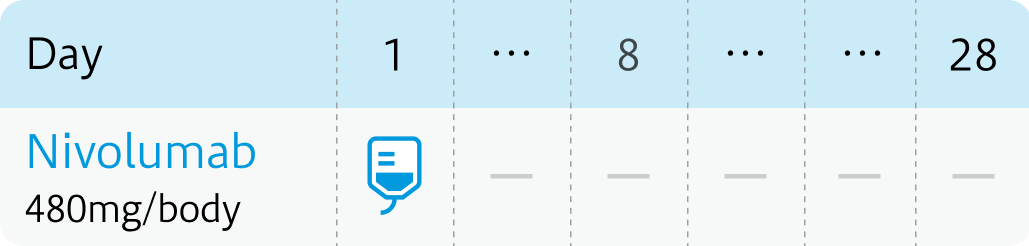
今回の追加承認は、 未治療の切除不能または転移性尿路上皮癌を対象に、 GC療法+ニボルマブとそれに続くニボルマブ単剤療法の有効性および安全性について、 GC療法単独を対照に比較検討した第Ⅲ相国際共同無作為化比較試験CheckMate 901の結果に基づく。
同試験において、 ニボルマブ併用群では化学療法単独に比べ、 全生存期間 (OS) および無増悪生存期間 (PFS) の有意な改善が示された (OS中央値 : 21.7ヵ月 vs 18.9ヵ月、 HR 0.78、 p=0.0171 / PFS中央値 : 7.9ヵ月 vs 7.6ヵ月、 HR 0.72、 p=0.0012)。
>> 関連レジメン
(HOKUTO編集部の関連コンテンツに遷移します)
1~6サイクル目

7サイクル目以降 (最長2年間)
シスプラチン
シスプラチン (商品名ランダ) は今回、 尿路上皮癌に対し、 ニボルマブとの併用における用量に関して一部変更承認された。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。