化学療法レジメン
5日前
【肺癌】コンパニオン診断薬 / 遺伝子パネル検査一覧 (5月14日更新)

肺癌領域のコンパニオン診断薬 (CDx) として承認されているマルチ・シングルプレックス検査および包括的がんゲノムプロファイリング (CGP) の最新情報をお届けします。
2026年5月14日版では、 ライブリバント®とリブロファズ®のEGFR遺伝子エクソン20挿入変異に対するCDxとして 「AmoyDx肺癌マルチ遺伝子PCRパネル」 が追加されました。
① マルチプレックスCDx
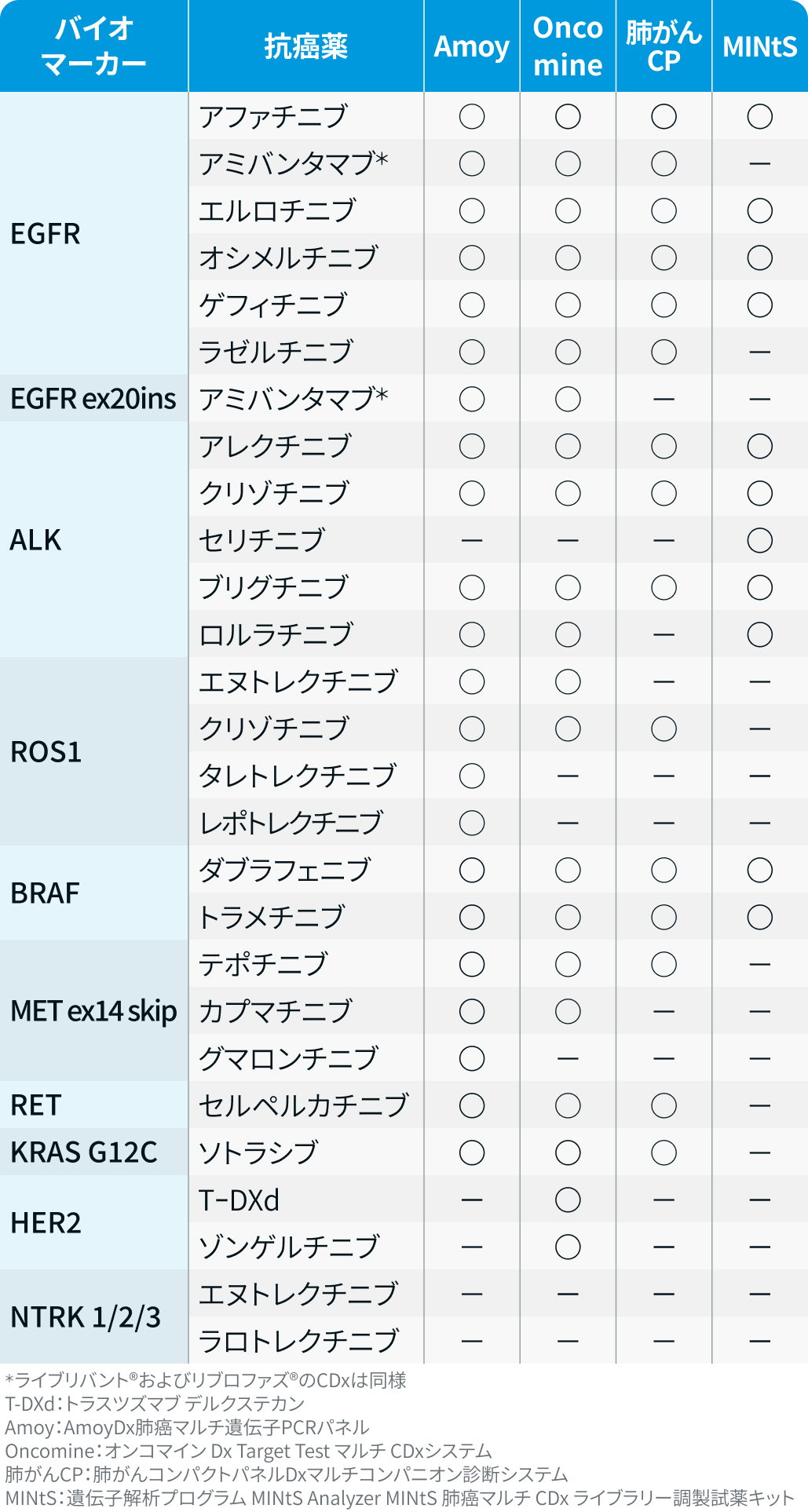
② シングルプレックスCDx
EGFRエクソン20挿入変異、 BRAF遺伝子変異、 METエクソン14スキッピング変異、 RET遺伝子変異、 HER2遺伝子変異、 およびNTRK1/2/3融合遺伝子に対しては、 いずれもシングルプレックスCDxは承認されていない。
EGFR遺伝子変異
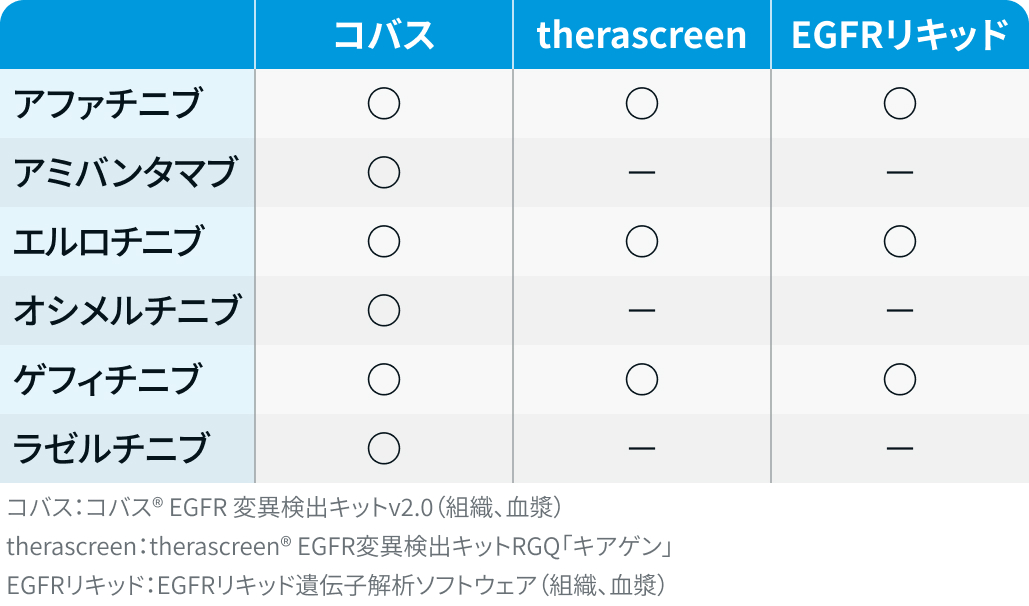
ALK融合タンパク・ALK融合遺伝子
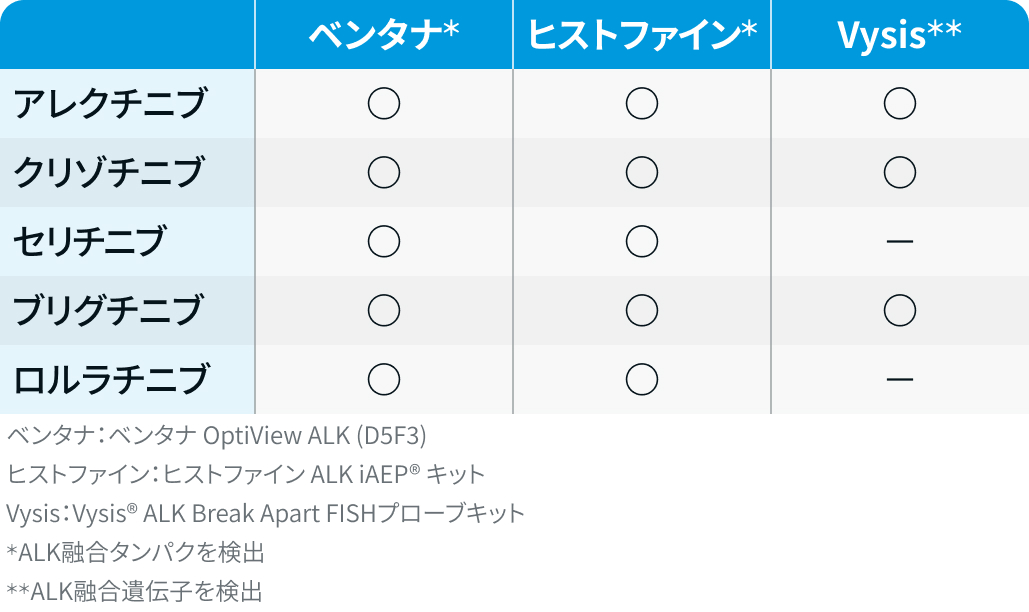
ROS1融合遺伝子

KRAS G12C遺伝子変異

PD-L1タンパク
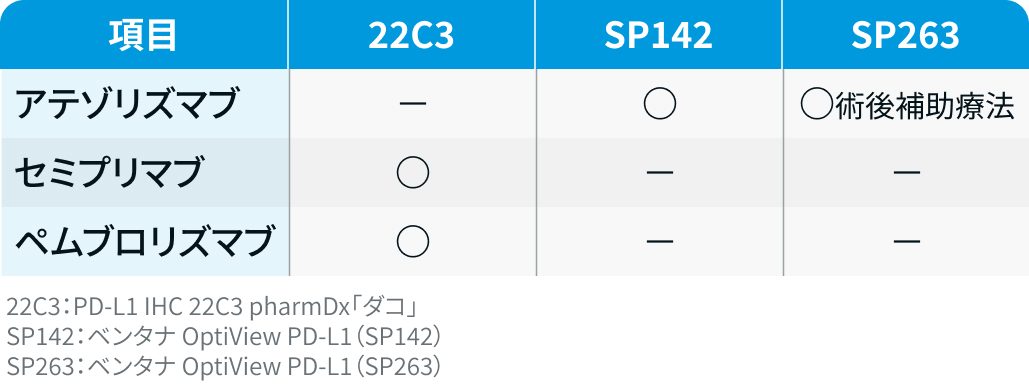
③ CDx承認のあるCGP検査
肺癌領域でCDxとして承認されている包括的がんゲノムプロファイリング (CGP) 検査は以下のとおり。
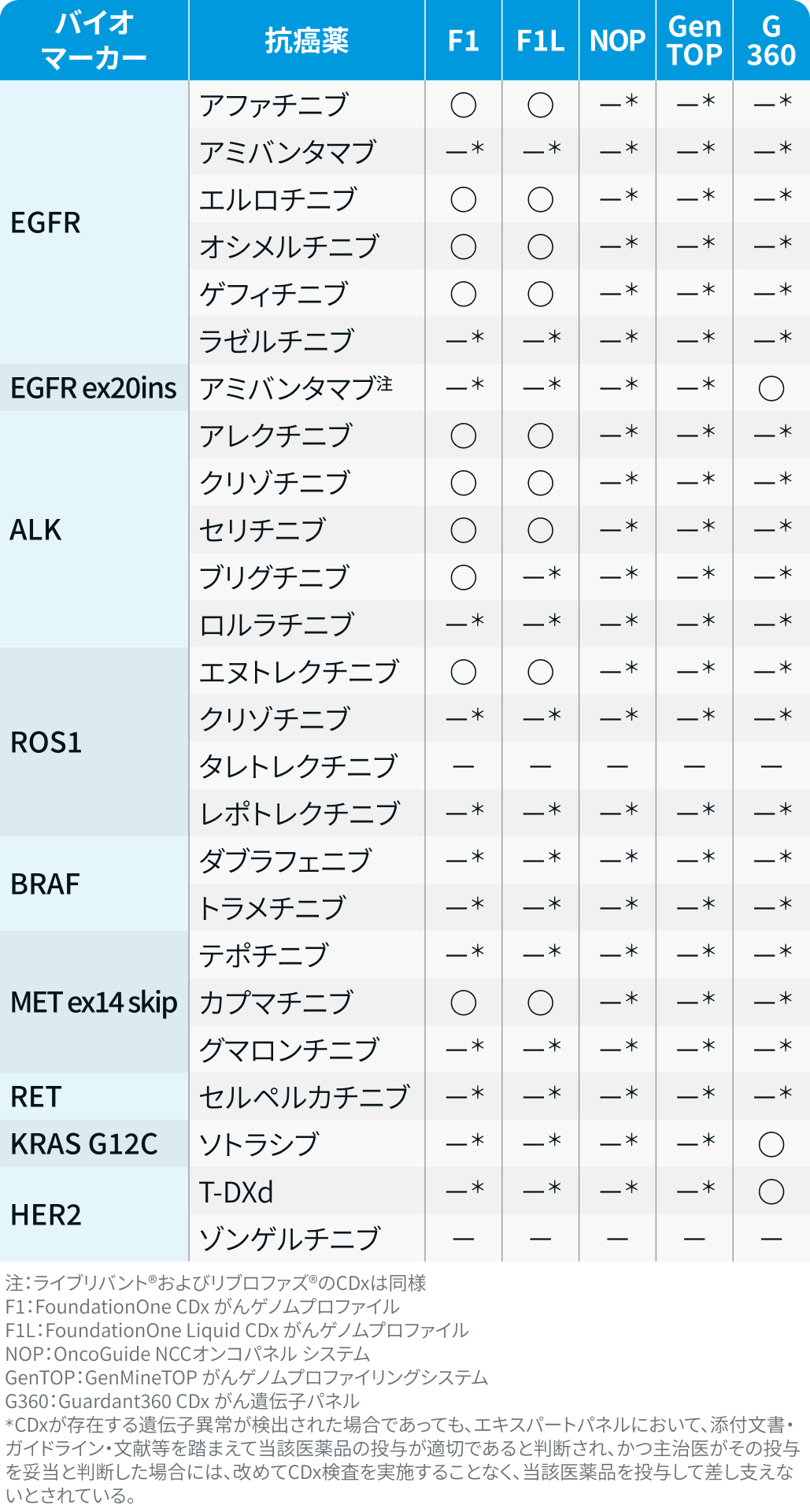
2025年6月11日、 日本癌治療学会・日本臨床腫瘍学会・日本癌学会の3学会合同ゲノム医療推進タスクフォース/ワーキンググループは、 一部の薬事未承認CDx対象バリアントに対し、 エキスパートパネル (EP) を経ずに薬剤投与を認める運用案を提言しており、 今後のEP運用の効率化が期待される。
出典
医薬品医療機器総合機構 (PMDA)
最新の情報については、 PMDA公式サイトでご確認ください。
【肺癌】コンパニオン診断薬 / 遺伝子パネル検査一覧 (5月14日更新)の全コンテンツは、医師会員限定でアプリからご利用いただけます*。
*一部のコンテンツは非医師会員もご利用いただけます
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
QRコードから
アプリを
ダウンロード!