HOKUTO編集部
2年前
癌領域で本邦初、 切除不能大腸癌へのプラグマティック臨床試験が開始
愛知県がんセンター薬物療法部医長の谷口浩也氏らの研究グループは本日 (12月25日) 、 前治療歴のある切除不能大腸癌患者を対象にしたトリフルリジン/チピラシル配合剤 (商品名ロンサーフ) +抗VEGFヒト化モノクローナル抗体ベバシズマブ併用療法 (FTD/TPI+Bmab) の投与方法について、 従来法と隔週法を比較する第Ⅲ相無作為化比較試験PRABITAS (試験番号 : jRCTs041230120) を開始したと発表した。 同試験は国内最大規模で実施され、 新たな試験手法である 「プラグマティック (実用的) 臨床試験」 が採用されていることが特徴となる。
背景
大腸癌に対するFTD/TPI+Bmab、 従来法における課題
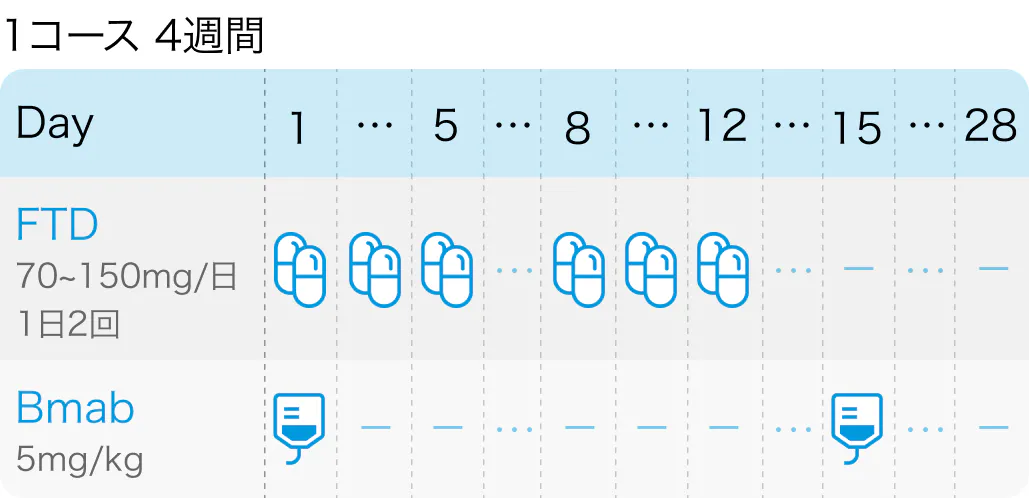
従来法としてのFTD/TPI+Bmabは、 28 日サイクルで行われ、 1日2回5日間のFTD/TPI内服と2日間の休薬を 2 回繰り返し、 その後 2 週間休薬する。 このレジメンは、 大腸癌に対する標準治療として既に承認されており、 世界中で用いられているが、 有害事象として白血球や好中球減少が比較的多く発現する。
そのため、 より安全かつ簡便な服用方法として隔週法 (14 日サイクルで行われ、 5日間の内服後に9日間休薬) が提案され、 小規模な臨床試験の結果から有害事象を軽減できる傾向が示された。 しかし、 隔週法の有効性と安全性はまだ十分に検証されていないため、 従来法と比較して隔週法が非劣性であるかどうかを明らかにする必要がある。
新たな手法 「プラグマティック臨床試験」 を採用
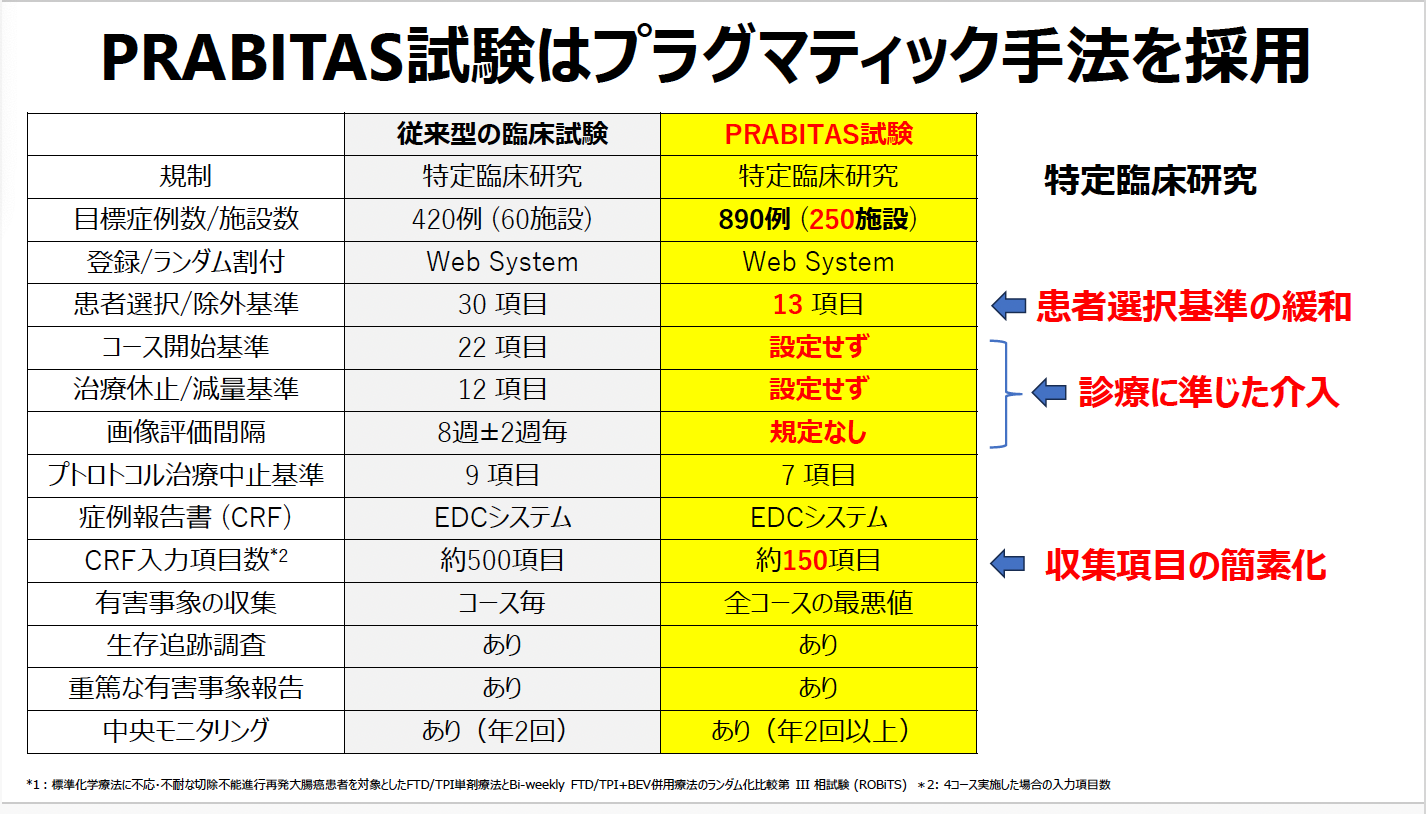
(谷口浩也氏提供)
隔週法の有効性と安全性を検証するためには無作為化比較試験 (RCT) が必要となるが、 従来のRCTは限られた条件下で手順を厳密に定めて行われるため、 科学的には妥当でも日常診療に必ずしも適用できるとは言い切れない。 そこで愛知県がんセンターは、 プラグマティック臨床試験 (以下、 PCT) という手法を用いて第Ⅲ相RCTを行うこととした。 癌領域でのプラグマティック臨床試験は、 国内初の試みとなる。
PCTの特徴は、 患者選択基準を緩和し、 実際の医療現場に近い集団を対象にして一般診療に近い環境で行われるため、 試験結果を日常診療での治療方針決定に活用できる点にある。 また、 参加医療機関からの情報収集を簡素化することで患者と医療者双方の人的・金銭的負担が大幅に軽減され、 結果的に治療開発の効率化ならびにコスト削減が期待できるという。
研究デザイン
対象
前治療歴*のある切除不能大腸癌で、 ECOG PSが0~2の患者 : 890例 (予定)
*フッ化ピリミジン、 オキサリプラチン、 イリノテカン、 血管新生阻害薬、 抗EGFR阻害薬 (RAS野生型)
試験期間
予定登録期間1年、 追跡期間1年、 総研究期間3年
介入
患者を以下の2群に1 : 1の割合で無作為に割り付ける。
- 隔週法 (14日サイクル) 群
FTD/TPIを1~5日目に経口投与+ベバシズマブを1日目に点滴投与し、 9日間休薬
- 従来法 (28日サイクル) 群
試験実施体制
全国約 250のがん診療連携拠点病院等に協力を依頼し、 協力両群とも実際の治療や検査は協力医療機関のもとで日常診療と同様に行う。
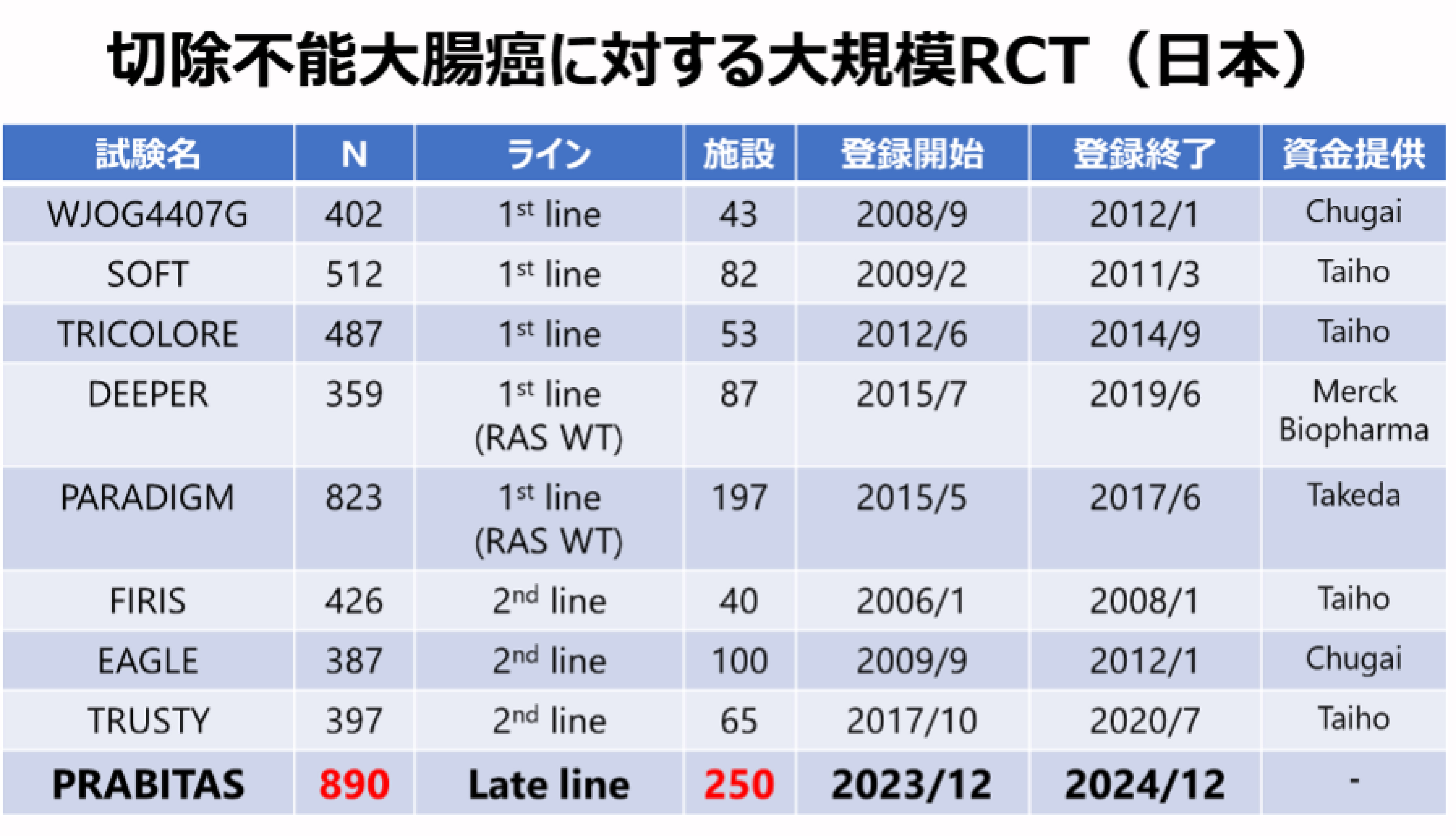
(谷口浩也氏提供)
主要評価項目
全生存期間 (OS)
副次評価項目
無増悪生存期間 (PFS)、 奏効割合 (RR)、 病勢制御割合、 治療成功期間、 有害事象
今後の展望
より安全で簡便な標準治療の提供実現なるか
同試験の結果、 前治療歴のある切除不能大腸癌患者に対する隔週法の有効性と安全性が明らかになれば、 患者に対して副作用が少なく、 かつ簡便な標準治療としてのFTD/TPI+Bmabを新たに提供できる。
また、 同試験によってPCTの有用性が示されれば、 患者・医療者双方の負担を軽減した効率的な治療開発の効率化、 ひいては活性化に繋がるという。
👨⚕谷口氏からのコメント
臨床研究法の制定以降、 リソースが多く必要とされるため、 医療者による臨床試験の実施は大幅に減少しました。 この試験がプラグマティックな手法を用いた効率的な臨床試験の有用性を示すことができれば、 医療者が解明したいクリニカルクエスチョンに最適な臨床試験手法の1つとして認識され、 「本来の臨床試験」 を取り戻すことができると考えています。
資金を提供できない中で、 本試験の趣旨に賛同し協力してくださる全国の医療機関と医療者の皆様に深く感謝申し上げます。
HOKUTOユーザー向けにコメントをいただきました。 誠にありがとうございました。
関連コンテンツ
隔週法
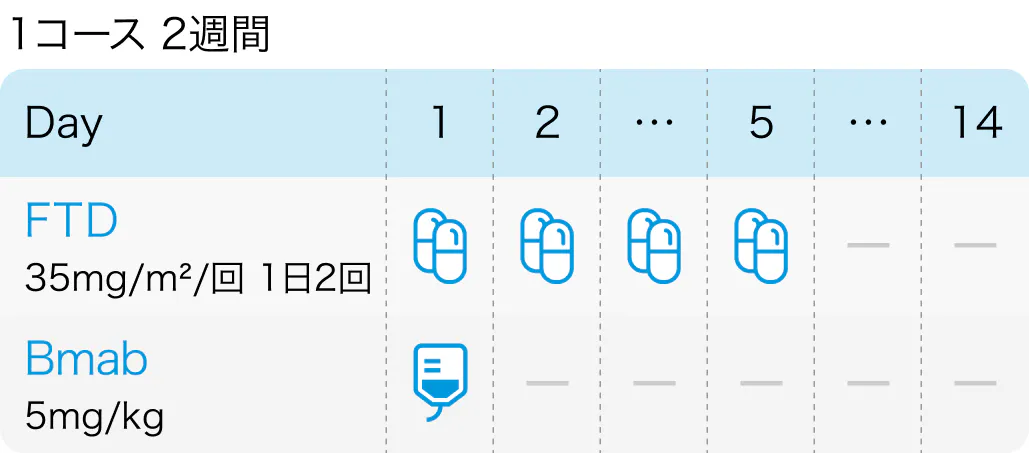
従来法
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。