HOKUTO編集部
3年前
FLT3-ITD陽性AMLの移植後維持療法、 ギルテリチニブでPFS延長せず

FLT3遺伝子内縦列重複 (FLT3-ITD) 変異陽性急性骨髄性白血病(AML)に対する造血幹細胞移植 (HSCT) 後の維持療法におけるFLT3阻害薬ギルテリチニブの有効性および安全性を検証した第III相国際共同プラセボ対照二重盲検ランダム化比較試験BMT-CTN 1506 (MORPHO) の主解析の結果から、 主要評価項目である無再発生存期間(RFS)の改善は認められなかった。 2023年6月8~11日に開催された欧州血液学会 (EHA 2023) において、 Johns Hopkins UniversityのMark J Levis氏が発表した。
試験の概要
対象
FLT3-ITD変異陽性のAMLで、 寛解導入療法後 (2サイクル以下) に初回完全寛解を達成し、 その後1年以内にHSCT施行予定の患者
方法
16カ国110施設において、 導入療法および強化療法後に488例を登録し、 HSCTを施行した。HSCT施行から30~90日以内に、 対象を以下の2群に1:1でランダムに割り付けた。
・ ギルテリチニブ120mg/日投与群:178例
・ プラセボ群:178例
造血幹細胞生着後から24カ月間投与を継続し、 定期的に微小残存病変 (MRD) を測定した
移植前、 ランダム化前、 移植後3、 6、 12、 18および24カ月後に検体 (骨髄穿刺液) 採取し、 PCR+NGS (次世代シーケンシング) を用いたFLT3-ITD変異を感度1×10⁻⁶以下で検出
評価項目
<主要評価項目> 無再発生存期間 (RFS)
<副次評価項目> 全生存期間 (OS)、 HSCT前後の微小残存病変(MRD)の有無がRFS、 OSに与える影響、 無イベント生存期間 (EFS)、 非再発死亡率、 急性および慢性移植片対宿主病 (GVHD)、 感染症の発症
結果
患者背景
ギルテリチニブ群、プラセボ群で同様であった
年齢中央値は両群とも53歳で、 男性の割合:51% vs 52% (ギルテリチニブ群 vs プラセボ群)、 アジア人:29% vs 33%、 MRD検出率はHSCT施行前10⁻⁴以上:22% vs 21%、 HSCT施行前10⁻⁶以上:47% vs 47%、 HSCT施行前または施行後10⁻⁶以上:50% vs 51%であった。
24カ月間の治療完了率
・ ギルテリチニブ群:52.8%
・ プラセボ群:53.9%
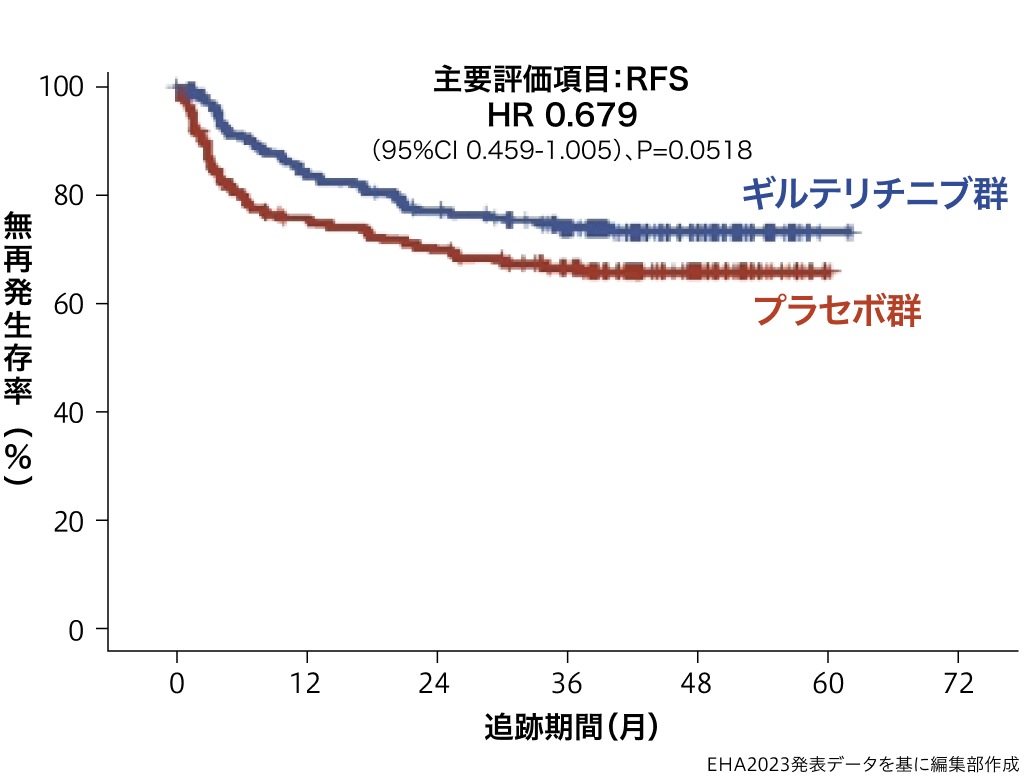
RFS(ITT解析)
イベント件数
・ ギルテリチニブ群:45件
・ プラセボ群:58件
2年RFS率 (95%CI)
・ ギルテリチニブ群:77.2% (70.1-82.8%)
・ プラセボ群:69.9% (62.4-76.2%)
HR: 0.679、95%CI 0.459-1.005、両側P=0.0518
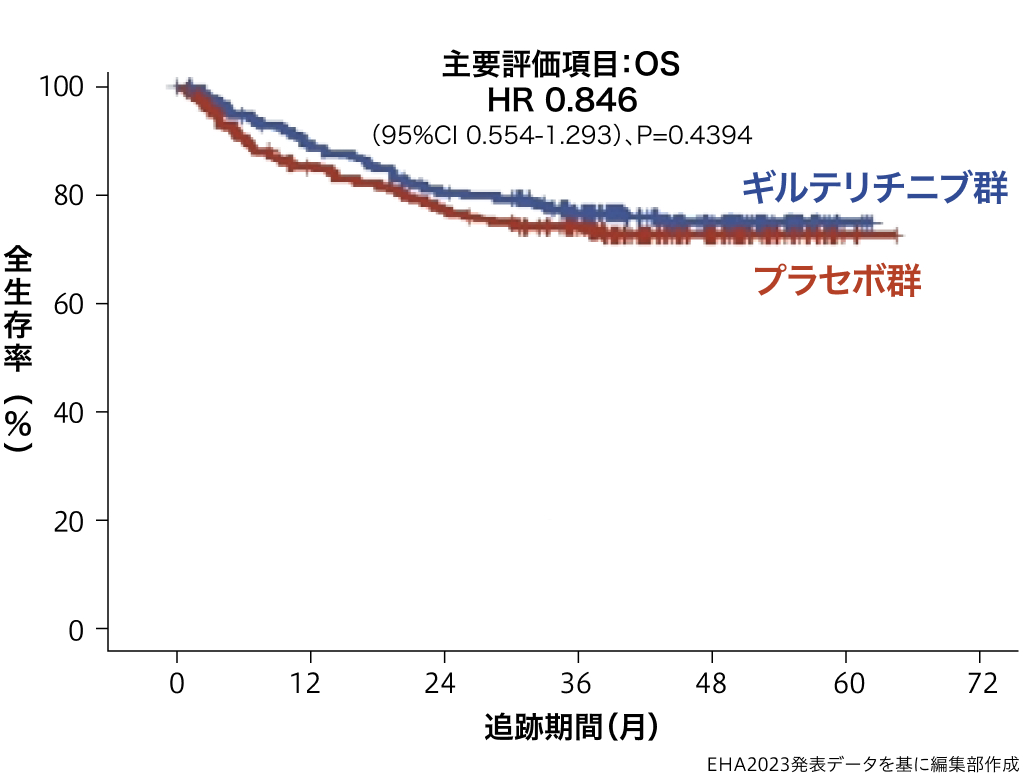
OS
イベント件数
・ ギルテリチニブ群:41件
・ プラセボ群:45件
HR 0.846 (95%CI 0.554-1.293)、 P=0.4394
RFSサブグループ解析
HSCT施行前または施行後のMRD (10⁻⁶以上) 検出の有無別
・MRD陽性群
HR 0.515 (95%CI 0.316-0.838)、 P=0.0065
・MRD陰性群
HR 1.213 (95%CI 0.616-2.387)、 P=0.575
OSサブグループ解析
HSCT施行前または施行後のMRD (10⁻⁶以上) 検出の有無別
・MRD陽性群
HR 0.514 (95%CI 0.331-0.798)、 P=0.0025
有害事象 (AE)
急性GVHD (グレード2-4)、 慢性GVHD
・ ギルテリチニブ群:18.5%、 52.2%
・ プラセボ群:20.3%、 42.4%
感染症 (グレード3以上)
・ ギルテリチニブ群:32.6%
・ プラセボ群:21.5%
薬剤関連TEAE (治験薬投与下のAE) による脱落、 治療中断、 グレード3以上
・ ギルテリチニブ群:15.2%、 18.0%、 61.2%
・ プラセボ群:7.9%、 6.8%、 25.4%
好中球減少 (24.7% vs 7.9%)、 血小板減少 (15.2% vs 5.6%)、 貧血 (6.2% vs 1.7%)
Levis氏らの結論
HSCT施行前後にMRDを検出したFLT3-ITD変異陽性AML患者では、 ギルテリチニブによるHSCT後維持療法は標準治療となりうる。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。