新薬承認情報
1年前
アナエブリ 「遺伝性血管浮腫」 適応に国内初承認-2月の承認情報まとめ-
7剤を承認、 うち新規有効成分1剤
医薬品医療機器総合機構 (PMDA) は、 2025年2月に7種類の医薬品が厚生労働省から承認を受けたと発表した。 (うち新有効成分は1剤)
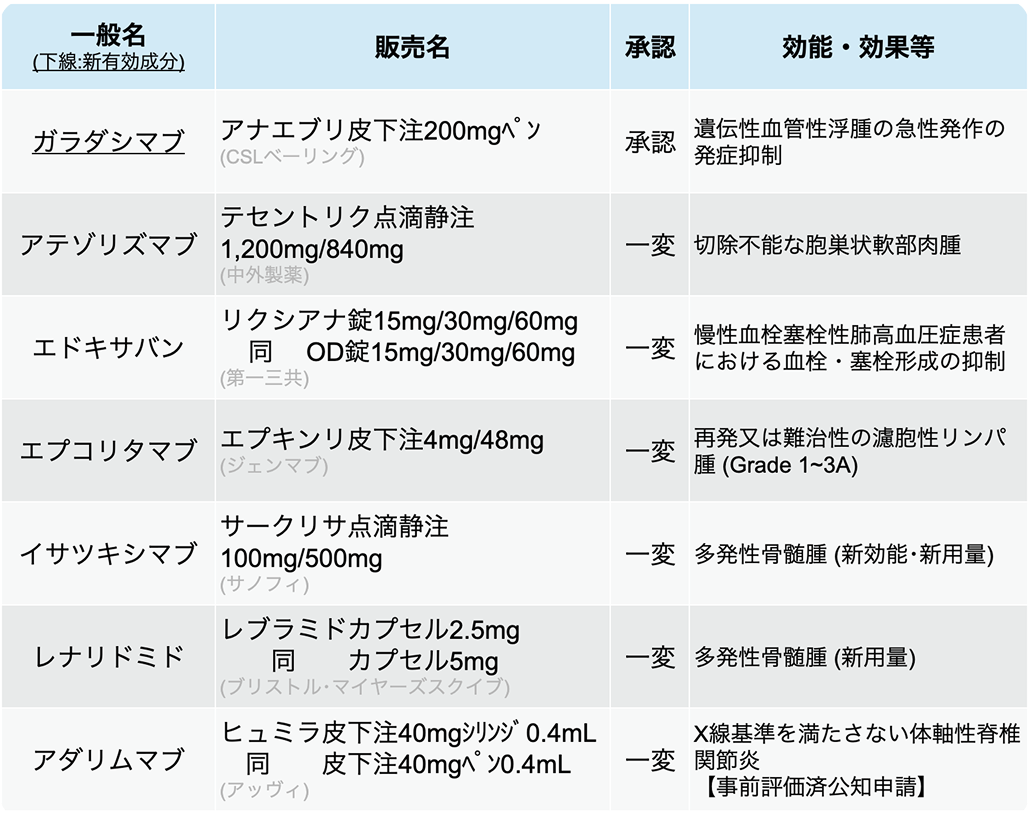
ガラダシマブ
ガラダシマブ (アナエブリ®) は、 活性化第XII因子 (FXIIa) を特異的に阻害する抗活性化第第XII因子抗体であり、 遺伝性血管性浮腫 (HAE) の急性発作の発症抑制を適応として日本で初めて承認された。 月1回の皮下投与が可能なプレフィルドペン製剤として利便性の向上が期待される。
今回の承認は、 日本人を含むタイプIまたはタイプIIのHAEを対象とした第III相国際共同試験VANGUARDおよび非盲検延長試験の結果に基づく。 VANGUARD試験では、 ガラダシマブの投与により、 1ヵ月あたりのHAE発作回数がプラセボ群と比較して有意に低下し (0.27ヵ月 vs 2.01ヵ月、 p<0.0001)、 安全性プロファイルは良好だった。
アナエブリ 「遺伝性血管浮腫」 適応に国内初承認-2月の承認情報まとめ-の全コンテンツは、医師会員限定でアプリからご利用いただけます*。
*一部のコンテンツは非医師会員もご利用いただけます
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
QRコードから
アプリを
ダウンロード!