HOKUTO編集部
2年前
【HER2CLIMB-02】tucatinib+T-DM1、HER2陽性既治療乳癌のPFS改善

前治療歴のあるHER2陽性局所進行/転移乳癌患者を対象に、 HER2チロシンキナーゼ阻害薬tucatinib+トラスツズマブ・エムタンシン (T-DM1) 併用療法の有効性および安全性を検証した第III相二重盲検プラセボ対照無作為化比較試験HER2CLIMB-02の結果、 tucatinib+T-DM1はT-DM1単独と比較して無増悪生存期間 (PFS) を有意に改善し、 脳転移患者におけるPFSも延長したことが示された。 米・Fred Hutchinson Cancer CenterのSara A. Hurvitz氏が発表した。
研究デザイン
対象
トラスツズマブとタキサン系薬による治療後に病勢進行を認めたHER2陽性局所進行/転移性乳癌で、 ECOG PS≦1の患者
脳転移に対し既治療で安定した症例および、 活動性または未治療の脳転移がある症例で、 即時の局所療法が必要でない患者も対象に含まれた。
方法
463例を以下の2群に1 : 1で割り付けた
- tucatinib群 (228例)
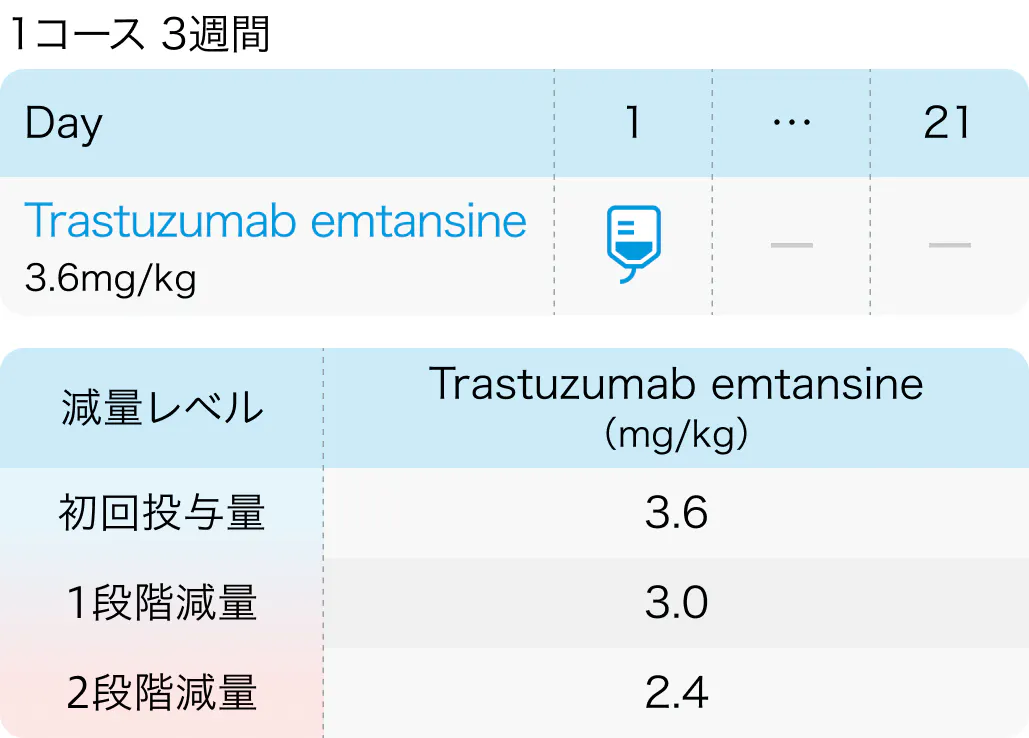
tucatinib 300mg 1日2回経口投与+T-DM1 3.6mg/kg静脈内投与
- プラセボ群 (235例)
プラセボ1日2回投与+T-DM1 3.6mg/kg静脈内投与
評価項目
主要評価項目
RECIST v1.1基準に基づく担当医の判定によるPFS
副次評価項目
全生存期間 (OS)、 RECIST v1.1基準に基づく確定客観的奏効率 (cORR)、 脳転移患者におけるPFSとOS
研究結果
追跡期間中央値
24.4ヵ月 (データカットオフ日 : 2023年6月29日)
患者背景 (tucatinib群、 プラセボ群)
- 年齢中央値 : 55.0歳、 53.0歳
- 女性 : 99.1%、 100%
- アジア人 : 30.7%、 27.7%
- ホルモン受容体陽性 : 60.1%、 59.6%
- 脳転移あり : 43.4% (活動期21.9%/治療により安定21.5%)、 44.7% (同24.3%/同20.4%)
PFS中央値
- tucatinib群 : 9.5ヵ月
(95%CI 7.4-10.9ヵ月)
- プラセボ群 : 7.4ヵ月
(95%CI 5.6-8.1ヵ月)
HR 0.76 (95%CI 0.61-0.95)、 p=0.0163
脳転移患者
- tucatinib群 : 7.8ヵ月
(95%CI 6.7-10.0ヵ月)
- プラセボ群 : 5.7ヵ月
(95%CI 4.6-7.5ヵ月)
HR 0.64 (95%CI 0.46-0.89)
cORR
- tucatinib群 : 42.0% (うち完全奏効は4.3%)
- プラセボ群 : 36.1% (同4.2%)
OS中央値
事前に規定されたOS最終解析のために必要なイベント253例中134例 (53%) が観察された段階で実施されたOS中間解析の結果では、 両群間で有意水準 (p≤0.0041) を満たさなかった。
- tucatinib群 : NR
(95%CI NR-NR)
- プラセボ群 : 38.0ヵ月
(95%CI 31.5ヵ月-NR)
HR 1.23 (95%CI 0.87-1.14)
安全性評価
新たな有害事象は認められず、 既報と一致していた。
Grade3以上の治療関連有害事象 (TEAE) の発現率
- tucatinib群 : 68.8%
- プラセボ群 : 41.2%
≧5%に認められたGrade3以上のTEAE (tucatinib群 vs プラセボ群)
- ALT上昇 : 16.5% vs 2.6%
- AST上昇 : 16.5% vs 2.6%
- 貧血 : 8.2% vs 4.7%
- 血小板減少 : 7.4% vs 2.1%
- 疲労 : 6.1% vs 3.0%
Sara A. Hurvitz氏らの結論
既治療のHER2陽性局所進行/転移乳癌患者において、 T-DM1にtucatinibを追加することでPFSが有意に改善した。 tucatinib群では肝イベントの発生率が高かったが、 一過性でコントロール可能、 かつ可逆的であった。 本試験は、 HER2陽性局所進行/転移性乳癌で脳転移例を含む患者において、 tucatinibを含むレジメンが病勢進行を遅らせることを証明した2件目の無作為化比較試験である。
(田中 理子)
関連コンテンツ
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。