Beyond the Evidence
3年前
【解説】切除不能大腸癌における抗EGFR抗体薬の再投与は有効か?
「Beyond the Evidence」 では、 消化器専門医として判断に迷うことの多い臨床課題を深掘りし、 さまざまなエビデンスや経験を基に、 より最適な解決策を探求することを目指す企画です。 気鋭の専門家による充実した解説、 是非参考としてください。
Clinical Question
切除不能大腸癌における抗EGFR抗体薬の再投与は有効か?
専門医の解説 「私はこう考える」

切除不能大腸癌における抗EGFR抗体薬の再投与はいくつかの第II相試験において有効性が報告されている。 しかし試験結果にばらつきがあること、 第II相試験の結果であること、 から現状で実臨床へそのまま外挿できるものではない。 ctDNAによる再投与直前のRAS status、 前治療の抗EGFR抗体薬への初期奏効、 前治療の抗EGFR抗体薬フリー期間は再投与の有効性を予測する重要な因子となる可能性があり、 これらを参考に再投与する対象を検討する。
抗EGFR抗体薬への感受性が復活するメカニズムとは
RAS野生型切除不能大腸癌においては抗EGFR抗体薬の上乗せが報告されており、 一次治療での細胞障害性抗癌剤との併用で特に左側大腸癌で標準治療となっている。
薬剤耐性と感受性復活のメカニズム
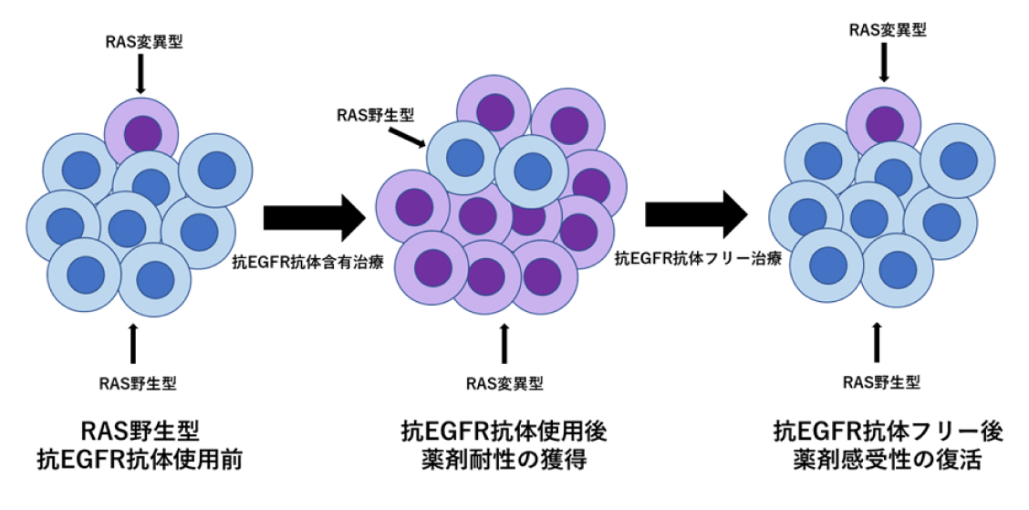
しかしながら、 抗EGFR抗体薬には薬剤耐性が生じることが報告されており、 この要因としてRAS野生型であっても検出されないRAS変異型が存在し、 抗EGFR抗体薬による治療後にこのRAS変異型が増殖することで、 薬剤耐性となる機序が報告されている(図1)。 こうした症例において、 2次治療で抗EGFR抗体薬でない治療を行うことで再度RAS野生型が増殖し、 抗EGFR抗体薬への感受性が復活するメカニズムが示唆されている。
第II相試験における有効性の報告
いくつかの第II相試験において抗EGFR抗体薬の再投与の有効性が報告されている(表1)。
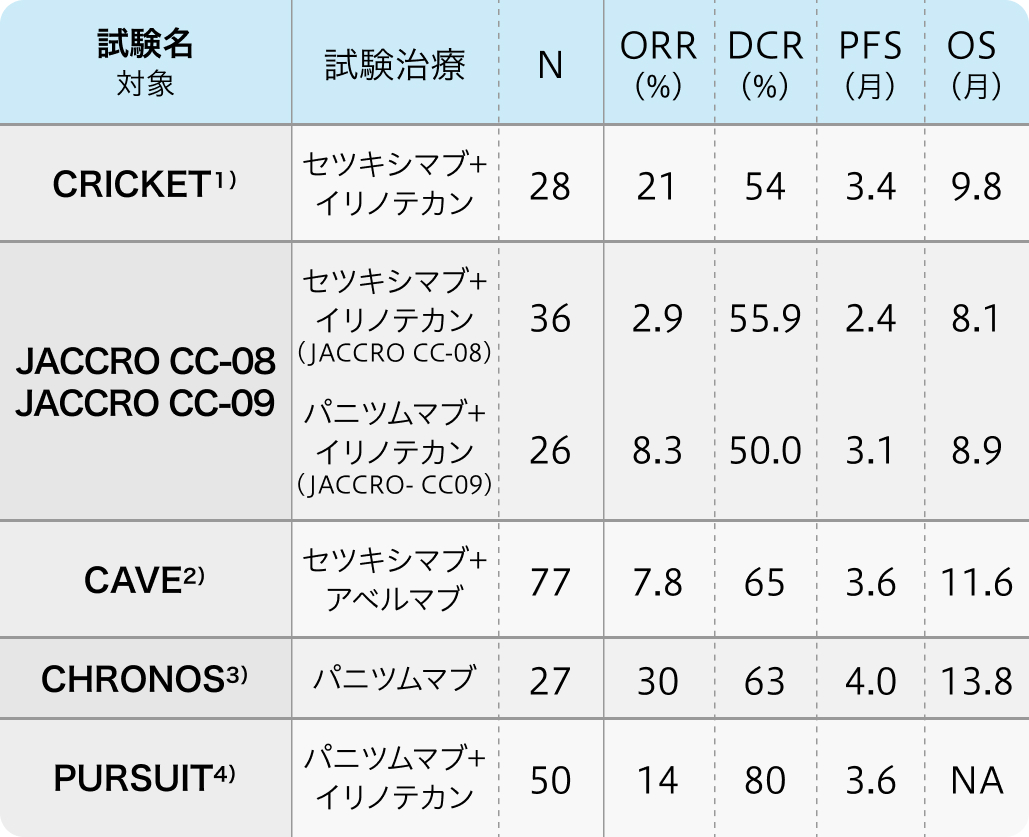
ORR: objective response rate, DCR: disease control rate, PFS: progression free survival, OS: overall survival
投与直前のRAS/BRAF statusの評価が重要に
RAS変異型では予後不良
CRICKET試験は1次療法でイリノテカン(IRI)+セツキシマブ(CET)含有レジメンで初期奏効が得られ、 2次治療でベバシズマブ(BEV)含有レジメンが使用された対象に3次治療としてIRI+CET再投与の有効性を検討した第II相試験である¹⁾。 奏効割合(ORR)は21%であり、 主要評価項目を達成した。 また副次評価項目である無増悪生存期間(PFS)と全生存期間(OS)中央値はともに3.4ヵ月と9.8ヵ月と良好な結果であった。
この試験においてはctDNAによる治療開始前のRAS statusが確認された。 subgroup解析で治療開始前のRAS野生型においてはPFSとOS中央値が4.0ヵ月、 12.5ヵ月とさらに良好な結果である一方、 RAS変異型では1.9ヵ月と5.2ヵ月と不良な結果であった。
RAS/BRAF変異型も予後不良
CAVE試験は1次治療でCETもしくはパニツムマブ(PANI)含有レジメンで初期奏効が得られ、 2次治療まで行われた対象に、 抗EGFR抗体薬の最終投与から4か月以上あけて、 CET+アベルマブの有効性を検討した第II相試験である²⁾。 主要評価項目であるORRは7.8%、 PFSとOS中央値は3.6ヵ月と11.6ヵ月と良好な結果であった。
この試験においても治療開始前にctDNAの測定がされており、 治療開始前のRAS/BRAF status別にsubgroup解析を行うとRAS/BRAF野生型においてPFSとOS中央値が4.1ヵ月、 17.3ヵ月と良好な結果である一方、 RAS/BRAF変異型では3.0ヵ月と10.4ヵ月と不良な結果であった。
これらの試験結果から、抗EGFR抗体薬の再投与の有効性および治療開始直前でのctDNA測定によるRAS/BRAF status評価の重要性が指摘された。
ctDNAガイド下の再投与は結果にバラツキ
上記の試験結果からイタリアで多施設共同第II相試験であるCHRONOS試験が行われている³⁾。 1次治療で抗EGFR抗体薬の使用歴かつ初期奏効があり、 治療開始前のctDNAでRAS/BRAF/EGFR野生型が確認されている対象で3次治療以降のPANI再投与の有効性が検討されている。 ORRは30%と主要評価項目を達成し、 PFSとOS中央値は4.0ヵ月と13.8ヵ月と良好な結果であった。
一方、本邦で行われた多施設共同第II相試験のPURSUIT試験は、 1次治療で抗EGFR抗体薬の使用歴かつ初期奏効があり、 治療開始前のctDNAでRAS/BRAF野生型が確認されている対象で3次治療以降のPANI+IRIの再投与の有効性が検討されている⁴⁾。 CRICKET試験とほぼ同じ対象であったが、 この試験ではORRが14%と低く、 主要評価項目を達成することができなかった。
これらの試験でctDNAガイド下での抗EGFR抗体薬の再投与が試されているが、 結果にはバラツキがあり、 不明な点も多い。 抗EGFR抗体薬の耐性機序として、 遺伝子異常以外の耐性機序が起きていることも細胞株を用いた研究で報告されており⁵⁾、 耐性機序のさらなる解明が切望される。
再投与を行うべき症例には検討が必要
さらに、いくつかの第II相試験で免疫チェックポイント阻害薬(ICI)と抗EGFR抗体薬、 イリノテカンなどの細胞障害性抗癌剤の3剤併用の再投与も検討されている。
CRACK試験はCET+リポソームイリノテカンに加えて、 抗PD-1抗体であるカムレリズマブの3剤併用療法の有効性を検討する第II相試験であった⁶⁾。 この試験ではORR 25%と主要評価項目を達成し、 かつPFSとOS中央値が6.9ヵ月と15.1ヵ月と良好な結果を示していた。 ICIを含めた3剤併用療法の再投与は奏効期間の延長を見込める可能性がある。 しかし小数例の第II相試験の結果であり、 今後のさらなる検討は必須である。
またRAS野生型の全症例に再投与の有効性があるわけではなく、 再投与を行うべき集団も検討が必要である。 前述のctDNAでの再投与直前のRAS statusに加え、 前治療での抗EGFR抗体薬への初期奏効、 前治療の抗EGFR抗体薬のフリー期間などは重要な因子となる可能性がある。 CRACK試験では前治療での抗EGFR抗体薬への初期奏効は必須でなく、 初期奏効が得られていない症例も含まれていた。 しかし前治療での抗EGFR抗体薬への初期奏効が得られていない症例においては3剤併用療法の再投与においても奏効が得られていなかった。
PURSUIT試験では、 PANI+IRIによる再チャレンジは抗EGFR抗体薬フリー期間が長い患者 (365日以上) で、 短い患者 (365日未満)より高いORR(37.5% vs. 9.5%, P=0.0037) となっていた。 この傾向はCRACK試験においても示されていた。 これらの3項目は抗EGFR抗体薬の再投与を検討する場合の参考となりえる。
切除不能大腸癌における抗EGFR抗体薬の再投与は有効性が一部報告されており、 今後も研究に注目が必要であるが、 全症例において検討できることでないことに留意すべきである。
参考文献
- Rechallenge for Patients With RAS and BRAF Wild-Type Metastatic Colorectal Cancer With Acquired Resistance to First-line Cetuximab and Irinotecan: A Phase 2 Single-Arm Clinical Trial. JAMA Oncol. 2019 Mar 1;5(3):343-350. PMID: 30476968
- Cetuximab Rechallenge Plus Avelumab in Pretreated Patients With RAS Wild-type Metastatic Colorectal Cancer: The Phase 2 Single-Arm Clinical CAVE Trial. JAMA Oncol. 2021 Oct 1;7(10):1529-1535. PMID: 34382998
- Circulating tumor DNA to guide rechallenge with panitumumab in metastatic colorectal cancer: the phase 2 CHRONOS trial. Nat Med. 2022 Aug;28(8):1612-1618. PMID: 35915157
- Kagawa Y, et al. Plasma RAS dynamics and anti-EGFR rechallenge efficacy in patients with RAS/BRAF wild-type metastatic colorectal cancer: REMARRY and PURSUIT trials. J Clin Oncol. 40: 16(suppl), 2022.
- Resistance Mechanisms to Anti-Epidermal Growth Factor Receptor Therapy in RAS/RAF Wild-Type Colorectal Cancer Vary by Regimen and Line of Therapy. J Clin Oncol. 2023 Jan 20;41(3):460-471. PMID: 36351210
- Cetuximab retreatment plus camrelizumab and liposomal irinotecan in patients with RAS wild-type metastatic colorectal cancer: Cohort B of the phase II CRACK study. Int J Cancer. 2023 May 10. doi: 10.1002/ijc.34531. PMID: 37163613
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。