HOKUTO編集部
3年前
エプコリタマブが再発・難治LBCLで承認 -9月の変更承認情報まとめ-
新規、 一部変更を含め23種類を承認
医薬品医療機器総合機構 (PMDA) は、 2023年9月に23種類の医薬品が厚生労働省から承認を受けたと発表した。 うち新薬は13剤であり、 残る9剤は一部変更承認およびバイオ後続品の承認である。
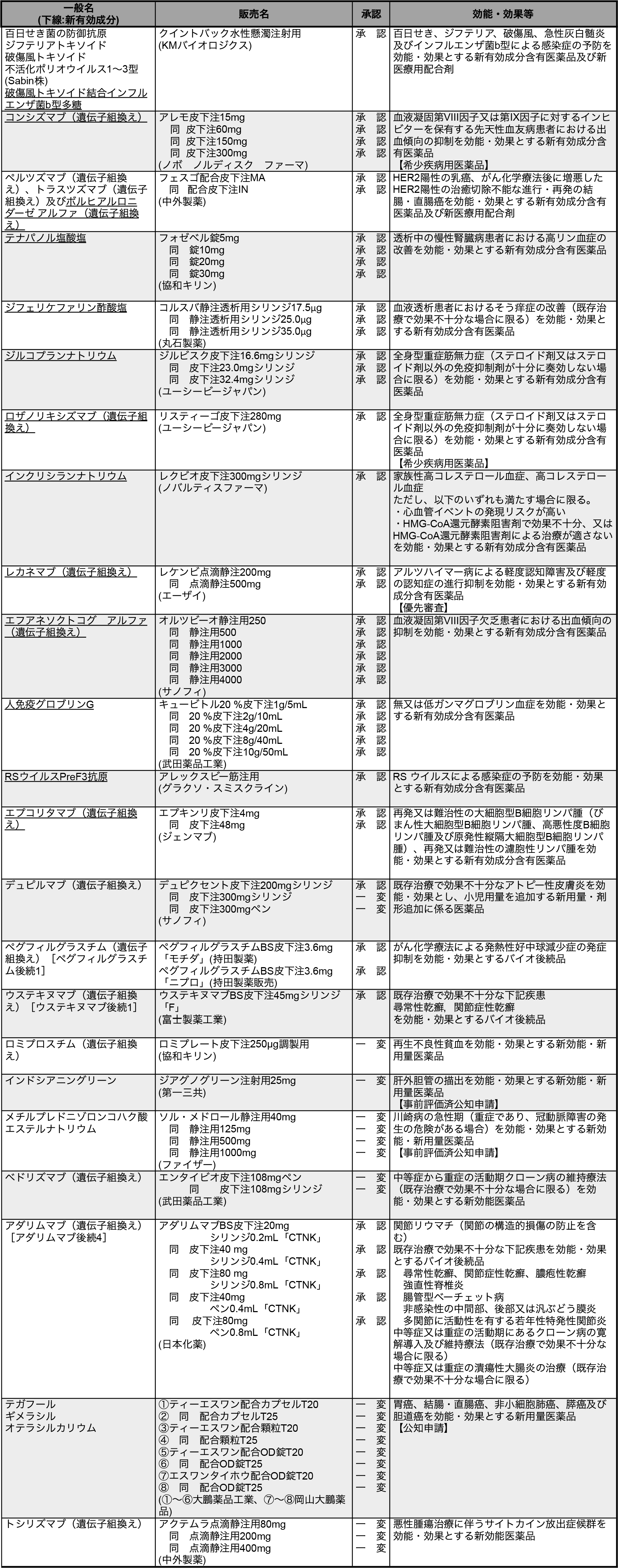
PMDA発表データを基に編集部作成
フェスゴ配合注
抗HER2抗体のペルツズマブとトラスツズマブの固定用量による配合皮下注製剤 (商品名フェスゴ配合皮下注 MA、 同IN)。 適応は、 「HER2陽性の乳癌」および「がん化学療法後に増悪したHER2陽性の治癒切除不能な進行・再発の結腸・直腸癌」である。 静脈注射剤では60~150分かけて投与するのに対し、 本皮下注射剤では5~8分以上で投与可能とされる。
エプコリタマブ
IgG1二重特異性抗体であるエプコリタマブ (商品名エプキンリ) は、 2 回以上の全⾝療法後に再発または難治性の⼤細胞型 B 細胞リンパ腫 (LBCL) のうちびまん性⼤細胞型 B 細胞リンパ腫 (DLBCL)、 ⾼悪性度 B 細胞リンパ腫 (HGBCL)、 原発性縦隔⼤細胞型 B 細胞リンパ腫(PMBCL)、 および再発または難治性の濾胞性リンパ腫 Grade 3B (FL3B) に対して、 承認された。 同薬は、 日本では、 ジェンマブが製造販売を⾏い、 アッヴィとのコ・プロモーションにより、 両社が情報提供活動を⾏っていく予定であるという。
エプコリタマブが再発・難治LBCLで承認 -9月の変更承認情報まとめ-の全コンテンツは、医師会員限定でアプリからご利用いただけます*。
*一部のコンテンツは非医師会員もご利用いただけます
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
QRコードから
アプリを
ダウンロード!