HOKUTO編集部
2年前
【MONARCH 3】HR+/HER2-未治療乳癌へのアベマシクリブ併用、OS延長も有意差示せず

ホルモン受容体 (HR) 陽性HER2陰性の進行乳癌患者を対象に、 1次治療における非ステロイド性アロマターゼ阻害薬 (NSAI) へのCDK4/6阻害薬アベマシクリブの上乗せ投与の有効性および安全性を検証した第Ⅲ相二重盲検試験MONARCH3の最終解析の結果、 アベマシクリブとNSAIの併用は、 NSAI単剤と比較して全生存期間 (OS) 中央値を13.1ヵ月延長したものの、 統計学的に有意な延長は認められなかったことが示された。 米・Mayo ClinicのMatthew P Goetz氏らが発表した。
背景
MONARCH3においては、 ホルモン受容体陽性HER2陰性進行乳癌の初回治療としてアベマシクリブ+NSAIの併用療法により、 無増悪生存期間 (PFS) の有意な改善が示された。 また、 2回目のOS中間解析では、 OS中央値に良好な差が認められていた。 今回は、 同試験におけるOSの最終解析結果が報告された。
研究デザイン
対象
未治療でホルモン受容体陽性HER2陰性の進行乳癌患者で、 以下の適格基準を満たすもの
- 閉経後
- 転移性または局所再発で、 全身療法歴なし
- 術前/術後療法を施行した場合、 終了後12ヵ月を超える無病生存期間あり
- ECOG PS (Performance Status) ≦1
方法
493例を以下の2群に1 : 1で割り付けた
- アベマシクリブ群 (328例)
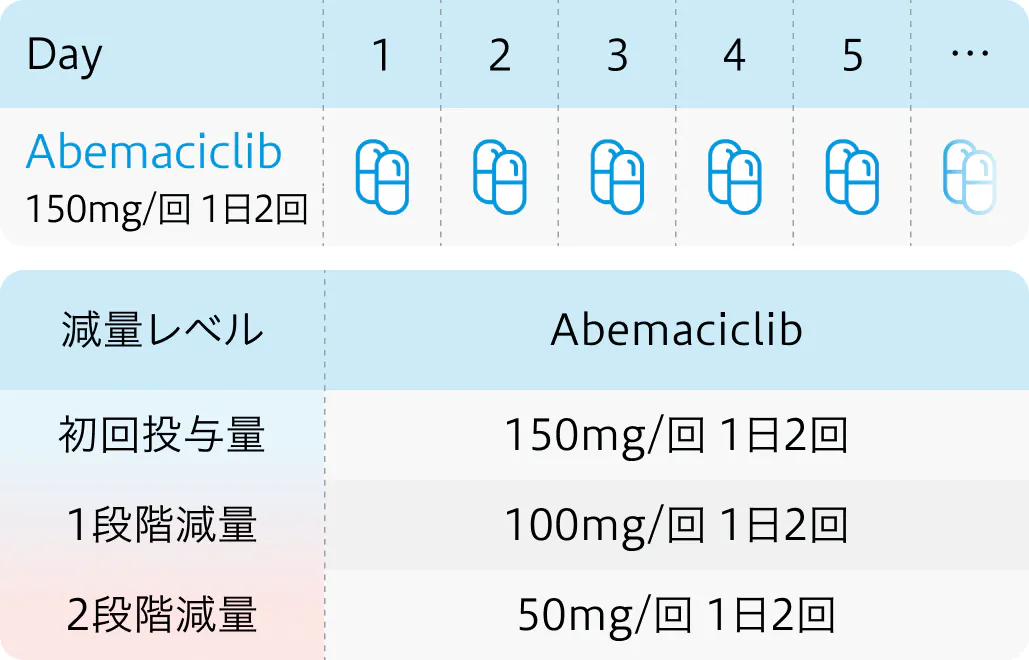
アベマシクリブ150mg 1日2回+NSAI (アナストロゾール1mgまたはレトロゾール2.5mg ) 1日1回を病勢進行 (PD) を認めるまで投与
- 化学療法群 (165例)
プラセボ1日2回+NSAI (アナストロゾール1mgまたはレトロゾール2.5mg) 1日1回をPDを認めるまで投与
評価項目
主要評価項目
担当医の判定によるPFS
副次評価項目
OS、 奏効率、 安全性
探索的評価項目
無化学療法生存期間 (CFS)
研究結果
追跡期間中央値
8.1年
PFS中央値 (ITT) の最終解析結果
- アベマシクリブ群 : 29.0ヵ月
- 化学療法群 : 14.8ヵ月
HR 0.535 (95%CI 0.429-0.668)、 nominal p≦0.0001
6年PFS率
- アベマシクリブ群 : 23.3%
- 化学療法群 : 4.3%
OS中央値 (ITT)
- アベマシクリブ群 : 66.8ヵ月
- 化学療法群 : 53.7ヵ月
HR 0.804 (95%CI 0.637-1.015)、 p=0.0664
OS中央値 (内臓転移を有する患者)
- アベマシクリブ群 : 63.7ヵ月
- 化学療法群 : 48.8ヵ月
HR 0.758 (95%CI 0.558-1.030)、 p=0.0757
CFS
- アベマシクリブ群 : 46.7ヵ月
- 化学療法群 : 30.6ヵ月
HR 0.693 (95%CI 0.557-0.863)、 nominal p=0.0010
安全性評価
アベマシクリブの長期投与による新たな安全性の懸念は認められなかった。
Grade3以上の治療関連有害事象の発現率
アベマシクリブ群 : 69%
プラセボ群 : 29%
Matthew P Goetz氏らの結論
最終解析の結果、 アベマシクリブとNSAIの併用療法はNSAI 単剤療法に比べ、 OS中央値をITT集団で13.1ヵ月、 内臓転移のあるサブグループで14.9ヵ月延長したものの、 両群に統計学的な有意差は認められなかった。 また、 アベマシクリブ併用療法はその後の化学療法開始を16.1ヵ月遅らせた。
今回の結果は、 ホルモン受容体陽性HER2陰性進行乳癌における1次治療としてのアベマシクリブ+NSAI併用療法を引き続き支持するものであり、 既報と一致していた。
(田中理子)
関連コンテンツ
サイクリン依存性キナーゼ (CDK) 4/6阻害薬
アロマターゼ阻害薬
【MONARCH 3】HR+/HER2-未治療乳癌へのアベマシクリブ併用、OS延長も有意差示せずの全コンテンツは、医師会員限定でアプリからご利用いただけます*。
*一部のコンテンツは非医師会員もご利用いただけます
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
QRコードから
アプリを
ダウンロード!