HOKUTO編集部
2ヶ月前
非扁平上皮NSCLCの術後ペメトレキセド、 適応外使用が保険適用に

日本肺癌学会は2月27日、 2024年2月に厚生労働省へ提出したペメトレキセド (商品名 アリムタ) の術後補助療法に対する 「医薬品の適応外使用事例申請書」 に関連して、 ペメトレキセドの 「非扁平上皮非小細胞肺癌 (病理病期Ⅱ-Ⅲ期) における術後補助療法」 に対する適応外使用の保険適用が認められた旨を同学会の公式サイトで発表した。
ペメトレキセドの適応外使用に係る保険診療上の取扱いについて
2月26日、 社会保険診療報酬支払基金が設置している 「審査情報提供検討委員会」 での検討において、 ペメトレキセドを 「非扁平上皮非小細胞肺癌 (病理病期Ⅱ-Ⅲ期) における術後補助療法」 に対して使用した場合、 当該使用事例を審査上認めるとの決定がなされたことが、 厚生労働省保険局医療課長から、 関連団体、 地方厚生(支)局医療課長等に通知された。
本邦において、 現在、 ペメトレキセドは以下の効能・効果について適応を有している。
- 悪性胸膜中皮腫
- 切除不能な進行・再発の非小細胞肺癌
- 扁平上皮癌を除く非小細胞肺癌における術前補助療法
上記通知では、 今回の適応外使用について審査上認める根拠を、 「薬理作用が同様であり、 妥当と推定される」 としている。
また、 留意事項として、 「非扁平上皮非小細胞肺癌 (病理病期Ⅱ-Ⅲ期) における術後補助療法」 に対する用法・用量が以下のとおり明記された。
通常、 成人にはペメトレキセドとして、 1日1回500mg/m²(体表面積)を 10分間かけて点滴静注し、 少なくとも20日間休薬する。 これを1コ ースとし、 投与を繰り返す。 なお、 患者の状態により適宜減量する。
外部サイトへ遷移します
病理病期Ⅱ-Ⅲ期非扁平上皮NSCLCの術後療法としてCDDP+PEM療法が可能に
上記に関連して、 本邦において、 「非扁平上皮非小細胞肺癌 (病理病期Ⅱ-Ⅲ期) における術後補助療法」 に対するシスプラチン+ペメトレキセド [CDDP+PEM] 療法が保険適用で使えることとなった。
CDDP+PEMのレジメン
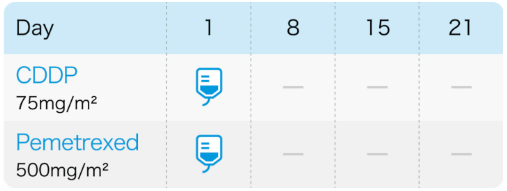
肺癌診療ガイドライン2024年版の4.周術期、 4-2術後補助化学療法のCQ27では、 上記レジメンに関連する試験結果が記され、 術後病理病期Ⅱ-ⅢB期 (第9版) 完全切除例に対してCDDP併用化学療法を行うよう強く推奨する根拠の一つとなっている。
JIPANG試験
完全切除非扁平上皮非小細胞肺癌Ⅱ-ⅢA期を対象として、 シスプラチン+ビノレルビン [CDDP+VNR] 療法とCDDP+PEM療法を比較した第Ⅲ相試験
同試験では、 CDDP+PEM療法のCDDP+VNR療法に対する優越性は示されなかったものの、 より良好な忍容性を示した¹⁾。
- 主要評価項目である無再発生存期間 (RFS) において、 CDDP+VNR療法に対するCDDP+PEM療法の優越性は示されなかった (37.3ヵ月 vs 38.9ヵ月、 HR 0.98 [95%CI 0.81-1.20]、 p=0.474)¹⁾
- 更新されたOSにおけるHRは1.03 (95%CI 0.80-1.32) であった²⁾
- Grade 3以上の有害事象の発現は、 全体で89.4% vs 47.4%であり、 発熱性好中球減少症は11.6% vs 0.3%、 貧血は9.3% vs 2.8%であった。 治療関連死亡は、 両群で1例ずつ認められた¹⁾
該当する臨床試験はこちら
J Clin Oncol. 2020 Jul 1;38(19):2187-2196
J Clin Oncol. 2023 Dec 1;41(34):5242-5246.
関連コンテンツ
抗悪性腫瘍薬 > 代謝拮抗薬
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。