HOKUTO編集部
2年前
【速報】レポトレクチニブ承認 : ROS1融合遺伝子陽性NSCLCへの新たな治療選択肢

本稿では肺癌領域における注目キーワードについて解説していく。 第6回となる今回は、2024年9月24日に国内承認されたROS1チロシンキナーゼ阻害薬 (-TKI) レポトレクチニブについて概説する (解説 : 国立がん研究センター中央病院呼吸器内科医長 吉田達哉先生)。
従来のROS1阻害薬の課題
ほとんどの症例で耐性を獲得
ROS1融合遺伝子陽性の非小細胞肺癌 (NSCLC) に対する治療薬は、 これまで、 ALK/ROS1阻害薬クリゾチニブおよびROS1/TRK阻害薬エヌトレクチニブが承認されていた。
一方、 これらの薬剤も他の分子標的薬と同様に、 初期は良好な治療効果を示すものの、 ほとんどの症例で耐性を獲得することが分かっている。
耐性獲得例の約1/3がROS1 G2032R変異
主な耐性機序としてはEGFR TKIにおけるEGFR T790M変異や、 ALK-TKIにおけるALK G1202R変異が知られているが、 ROS1においてはROS1 G2032R変異が認識されている (図1)¹⁾。
▼図1 クリゾチニブ治療後のROS1耐性変異の頻度

出典1を基に編集部作成
耐性を克服した薬剤開発が急務
さらに、 ROS1陽性NSCLCは、 ALK陽性NSCLCほど頻繁ではないものの、 既存のROS1-TKI治療中に脳転移で増悪する患者が少なくない。 そのため、 既存のROS1-TKIの耐性を克服し、 かつ頭蓋内病変にも効果を発揮する次世代のROS1-TKIの開発が求められてきた。
次世代型ROS1-TKIの開発
注目薬剤 : レポトレクチニブ
本邦では、 レポトレクチニブ、 taletrectinib、 zidesamtinibなど、 複数の次世代ROS1-TKIの開発が進められている。
その中でもレポトレクチニブは、 ROS1 G2032R耐性変異に対して有効性を示し、 頭蓋内奏効性も高い次世代のROS1 (およびTRK) -TKIである²⁾。 その安全性および有効性は、 第Ⅰ/Ⅱ相TRIDENT-1試験で報告されている³⁾。
治療歴にかかわらず、 良好な治療成績
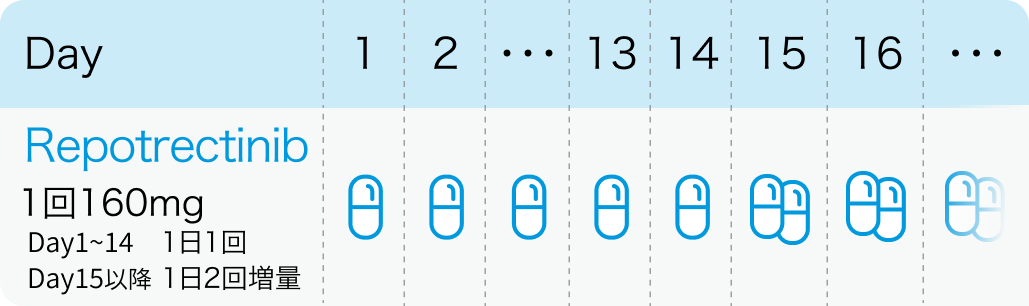
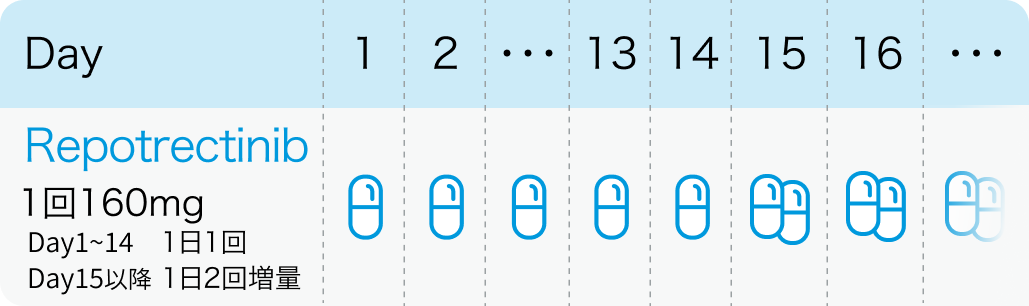
第Ⅰ相TRIDENT-1の結果、 レポトレクチニブの推奨用量は160mgを1日1回、 14日間投与後に160mgを1日2回とされた。
第Ⅱ相TRIDENT-1の結果、 ROS1-TKIによる治療歴のないROS1陽性NSCLC71例において、 レポトレクチニブの奏効割合 (部分奏効+完全奏効) は79% (95%CI 68-88%)、 奏効期間中央値は34.1ヵ月 (同 25.6ヵ月-評価不能) だった。
また、 1種類のROS1阻害薬による治療歴があり、 化学療法歴のないROS1陽性NSCLC56例では、 奏効割合 (部分奏効+完全奏効) は38% (95% CI 25~52%)、 奏効期間中央値は14.8ヵ月 (同 7.6ヵ月-NE) だった (図2) 。
▼図2 奏効割合
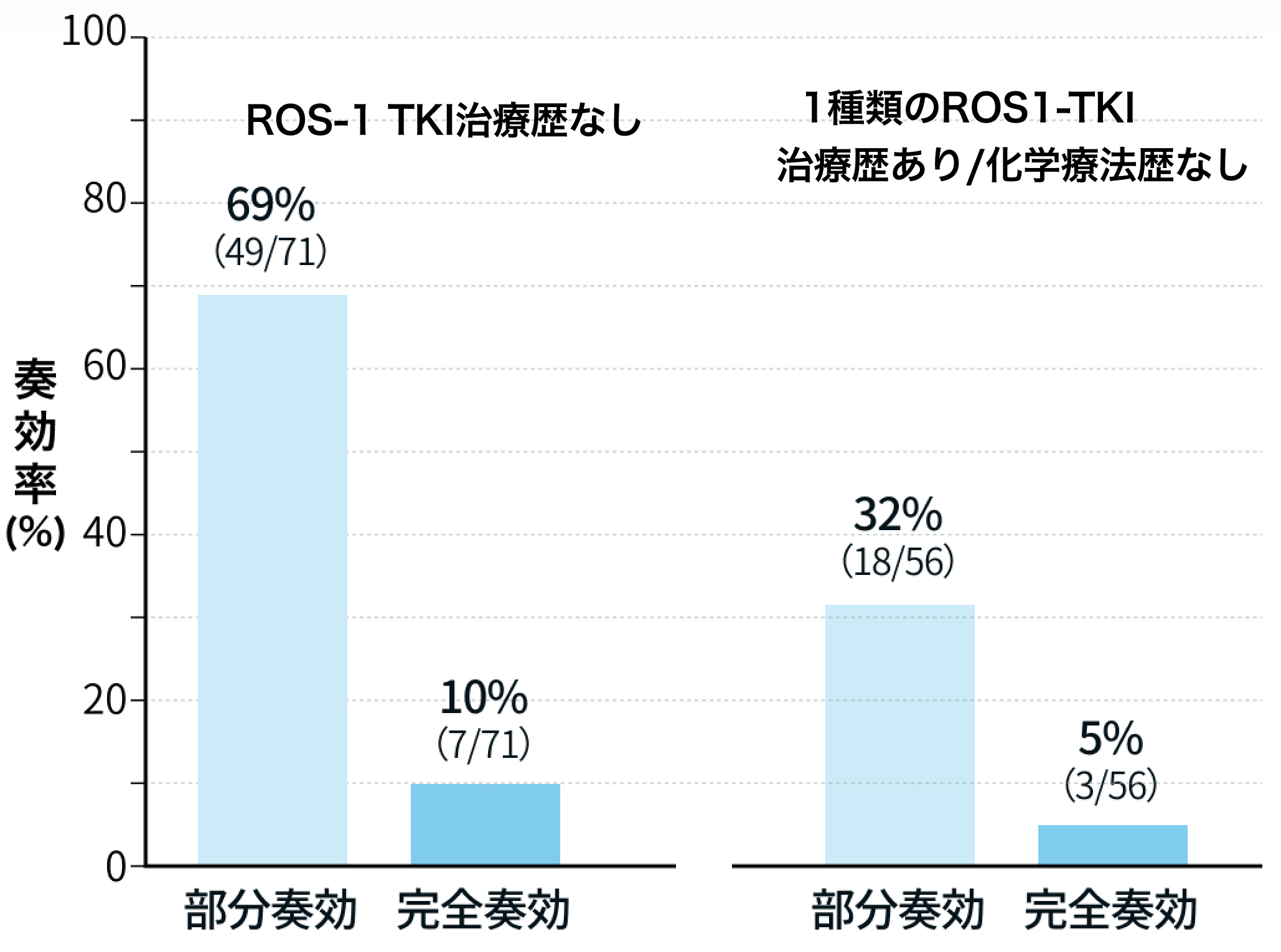
出典3を基に編集部作成
無増悪生存期間 (PFS) 中央値は、 ROS1-TKIによる治療歴のない集団で35.7ヵ月 (同 27.4ヵ月-NE)、 1種類のROS1阻害薬による治療歴があり化学療法歴のない集団で9.0ヵ月 (同6.8-19.6ヵ月) で、 12ヵ月PFS率はそれぞれ77%、 41%だった (図3)。
▼図3 両集団のPFS率
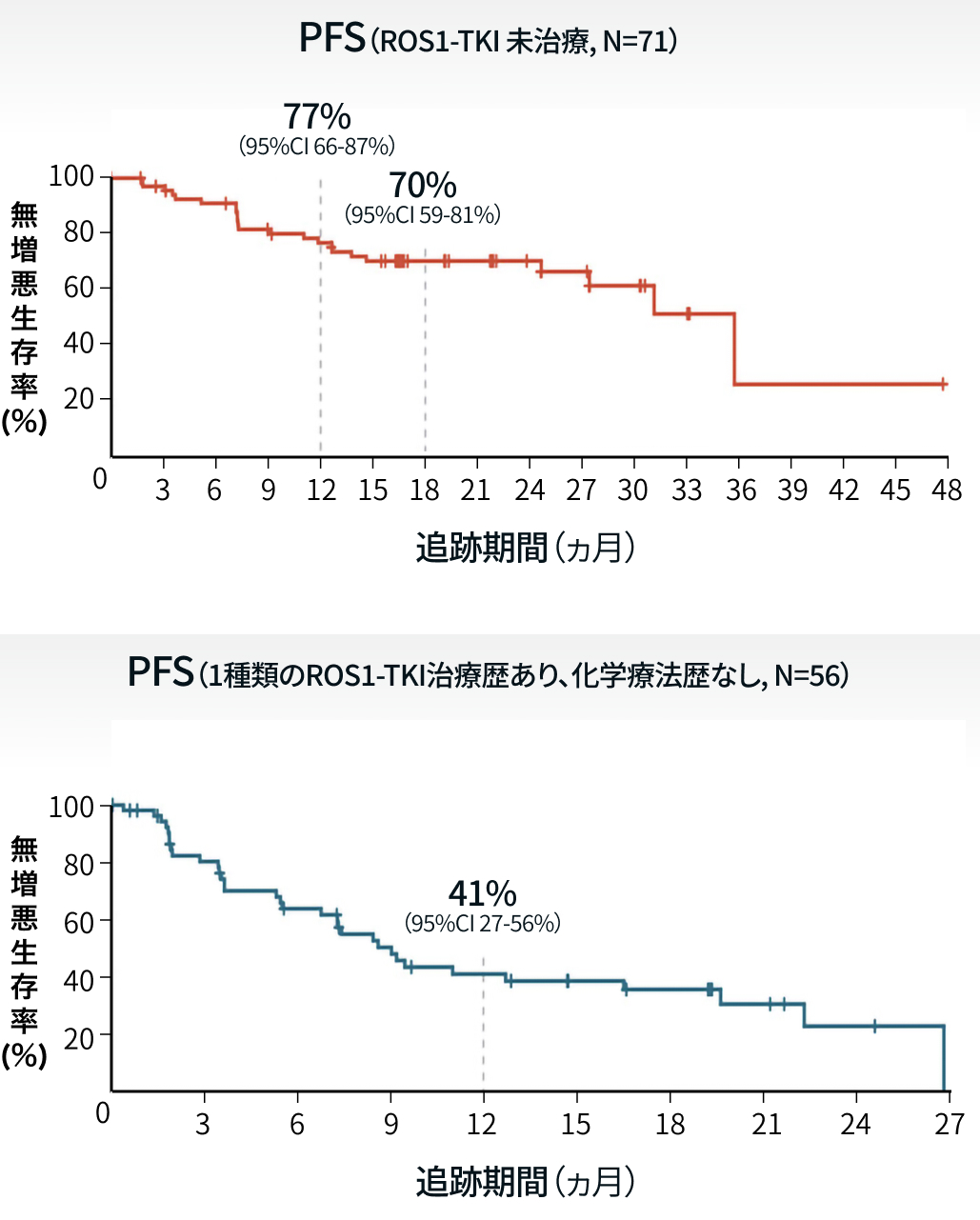
出典3を基に編集部作成
さらに、 ROS1 G2032R変異を有する患者17例に対する客観的奏効率は59% (95%CI 33-82%) だった。
以上の結果から、 レポトレクチニブはROS1-TKIによる治療歴にかかわらず、 良好な治療成績を示すことが明らかにされた。
ほぼ全例に有害事象が発現
安全性については、 ほぼすべての症例で何らかの有害事象が認められた。 中でも浮動性めまい (58%)、 味覚異常 (50%)、 感覚異常 (30%) が特徴的だった (図4)。 また、 35%で治療関連有害事象によるレポトレクチニブの減量が必要となり、 3%の患者で投与が中止された。
▼図4 主なレポトレクチニブの有害事象
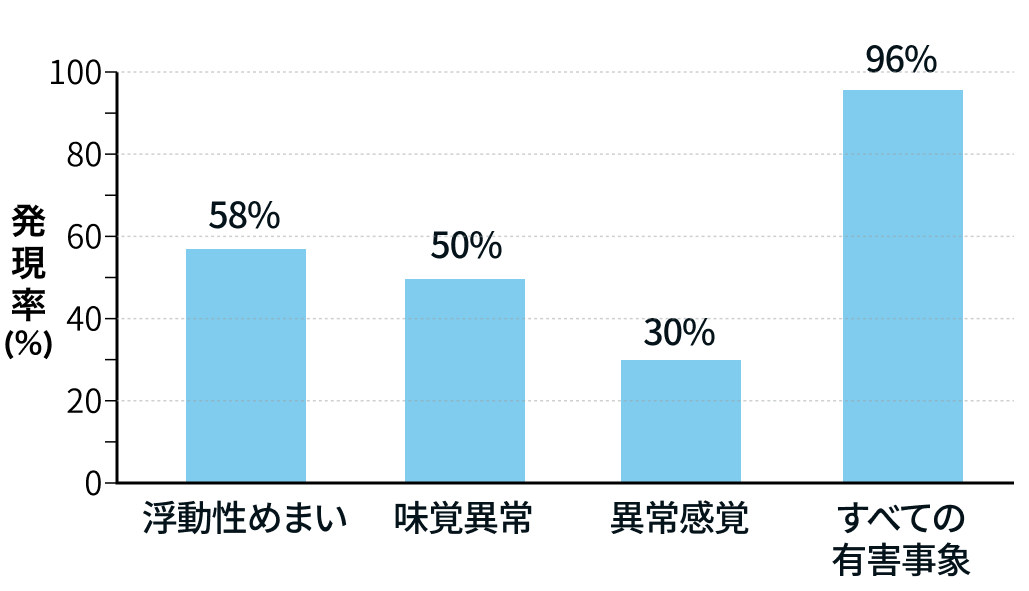
出典3を基に編集部作成
日本においても承認
2024年9月24日、 レポトレクチニブはROS1陽性の切除不能な進行・再発のNSCLCを効能または効果として、 本邦で承認された。 今後、 新たな治療選択肢となることが期待される。
解説医師

出典
¹⁾ Clin Cancer Res. 2021;27(10):2899-2909.
²⁾ Cancer Discov. 2018;8(10):1227-1236.
³⁾ N Engl J Med. 2024;390(2):118-131.
関連コンテンツ
NSCLC (遺伝子変異/転座+) > ROS1融合遺伝子陽性
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。