HOKUTO編集部
1年前
【解説】第3のFGFR阻害薬、 タスルグラチニブの実力は?

胆道癌におけるFGFR2融合遺伝子/再構成に対するFGFR阻害薬の有効性が示されており、 本邦ではこれまでに、 ペミガチニブ (ペマジール®) とフチバチニブ (リトゴビ®) の2剤が承認されている。
本稿では、 2024年9月に新たに国内承認となったタスルグラチニブ (タスフィゴ®) について、 新規コンパニオン診断であるFISH検査 (Fluorescence In Situ Hybridization) を含めて解説する。
FGFR融合遺伝子異常、 ペミガチニブ、 フチバチニブについては連載第2回を参照されたい。
タスルグラチニブ (タスフィゴ®)
タスルグラチニブはFGFR1~3を対象とし、 ATP競合性の可逆的阻害を示す薬剤である。 本薬の有効性および安全性については、 化学療法歴のある切除不能な胆道癌患者を対象とした非盲検単群第II相試験E7090-J000-201¹⁾が行われている。
E7090-J000-201試験では、 FISH検査によるFGFR2融合遺伝子もしくは再構成のプレスクリーニングが行われている。 FGFR2遺伝子融合/再構成 (63例)における奏効割合が30%、 全生存期間中央値が13.1ヵ月だった。
本試験の結果から、 FGFR2遺伝子融合/再構成を有する胆道癌におけるタスルグラチニブの有効性が示され、 承認されている。 なお、 CDx検査にはFISH検査 (AmoyDx® FGFR2 Gene Break-apart FISH) が用いられている。
関連コンテンツ
FGFR阻害薬3剤の比較 : 3つの視点
▼有効性
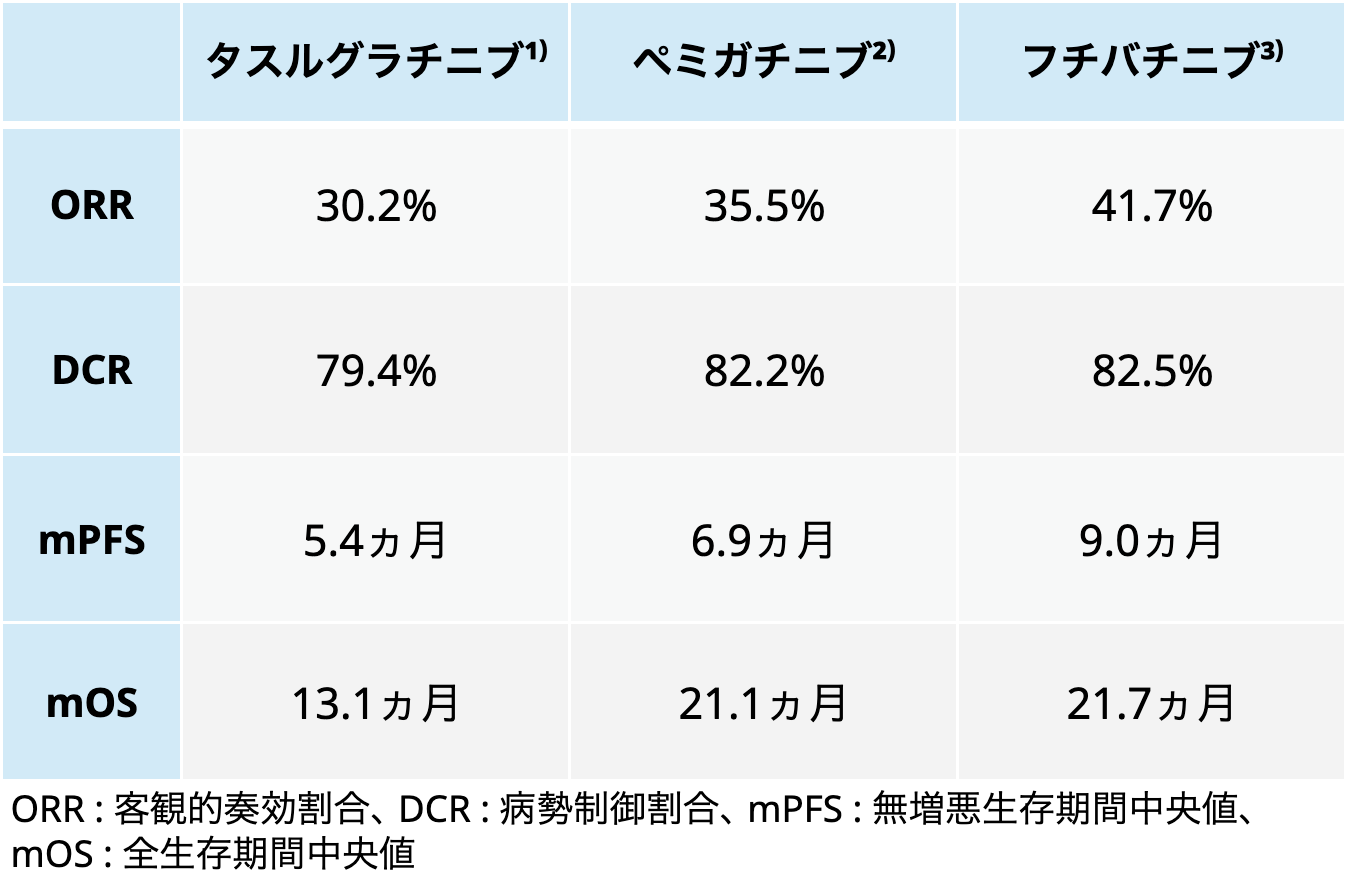
▼有害事象の発現

▼治療ライン別のORR
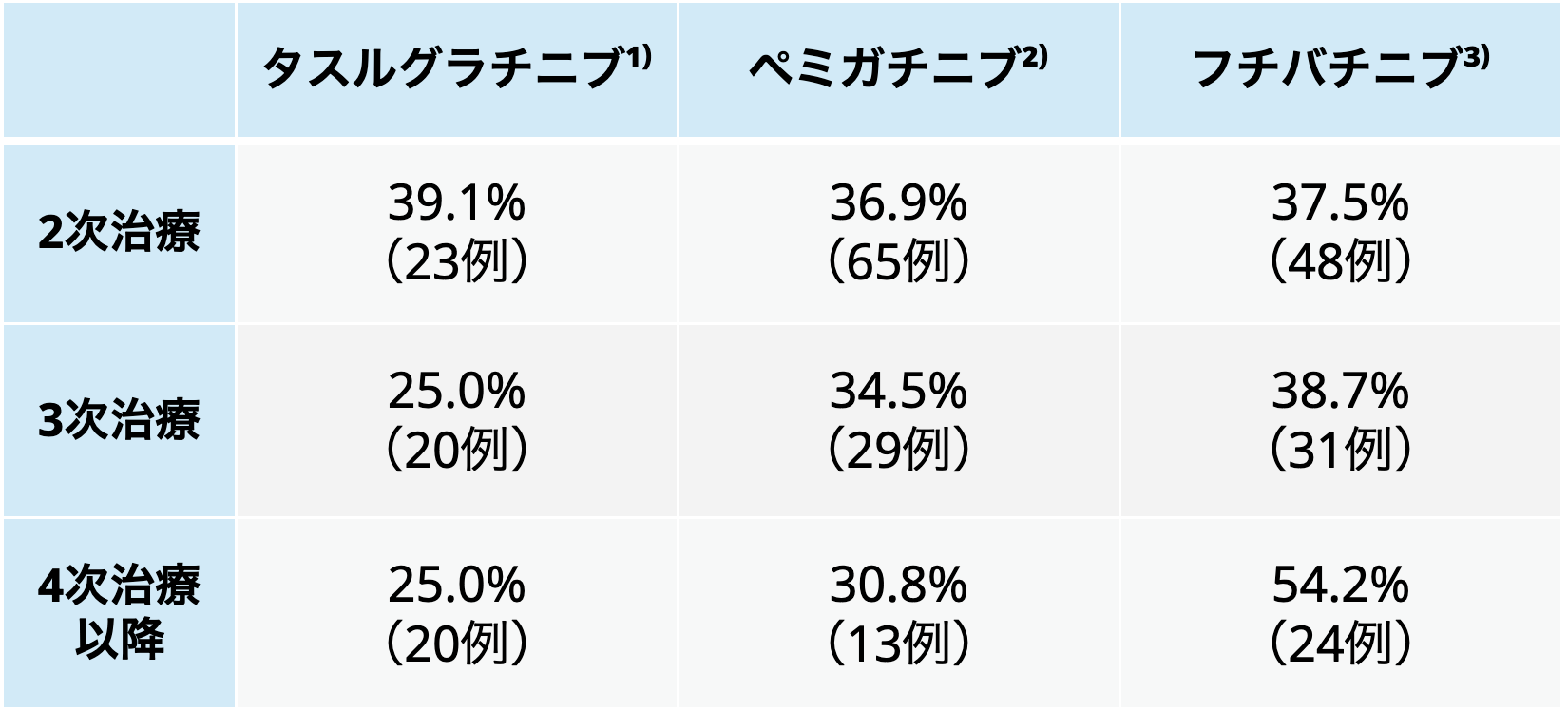
タスルグラチニブはその他のFGFR阻害薬と比較して、 有効性が劣っている可能性が指摘される。 しかし、 タスルグラチニブの第II相試験では3次治療以降に投与されている患者が60%程度含まれており、 OSにおける差はこの点が大きく影響していると考える。
また、 2次治療のみのORRではその他の薬剤と差がみられていない。 異なる臨床試験を比較することは許容されないことから、 上記の比較データはあくまで参考資料として考えるべきある。 FGFR阻害薬の使用に関しては、 今後の実臨床におけるデータが重要である。
新規コンパニオン診断 : FISH検査
「AmoyDx® FGFR2 Break-apart FISHプローブキット」は、 切除不能進行/転移性FGFR2陽性胆道癌に対するFGFR阻害薬タスルグラチニブのコンパニオン診断として2024年8月26日に国内承認された。
FISH検査の特徴として、 結果が得られるまでの時間が短い点と、 少ない組織量での検査が可能である点が挙げられる。
現在、 報告されている情報では、 必要な組織は3~5μmの厚さに薄切されたスライド3枚、 結果返却までの所要日数は8~15日である⁴⁾。
また、 FISH検査の実施時期は既定がないため、 胆道癌の診断後で薬物療法開始前にFGFR2融合遺伝子の可能性を検討することが可能である。
本検査が承認されたことで、 診断時に得られる組織量が少なく遺伝子パネル検査ができない患者にも、 FGFR2融合遺伝子の有無を確認する方法が新しく提供された。
FISH検査は、 そのほかの薬剤のコンパニオン診断に用いられる遺伝子パネル検査と比較して、 検体が少なく済み、 結果が返却されるまでの所要日数が短いという利点がある。
本検査は、 組織採取が困難であることが多い肝門部領域胆管癌などでは大変重要な検査である。
一方で、 FISH検査はFGFR2融合遺伝子の確認のみに特化しているため、 その他の治療標的遺伝子を確認できない点は欠点である。
おわりに
タスルグラチニブは本邦における第3のFGFR阻害薬であり、 FISH検査がコンパニオン診断であることが最大の特徴といえる。 これまでのFGFR阻害薬ではカバーできていないFGFR2融合遺伝子/再構成を認める患者に対する、 有効な薬剤となる可能性が期待される。
<出典>
1) J Clin Oncol. 2024 Jan 22;42(3_suppl):471.
2) Lancet Oncol. 2020 May;21(5):671-684.
3) N Engl J Med. 2023 Jan 19;388(3):228-239.
4) エスアールエル社2024年12月発表資料 : SRL NEWS FGFR2融合遺伝子 (FISH) .

修正履歴(2026年1月6日):タスルグラチニブの臨床試験名で「FOENIX-CCA2」とあったのは「E7090-J000-201」の誤りでした。お詫びして訂正します。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。