新薬承認情報
2年前
パドセブ 「尿路上皮癌」 等が適応へ-9月の承認情報まとめ-
34剤を承認、 うち新規有効成分は14剤
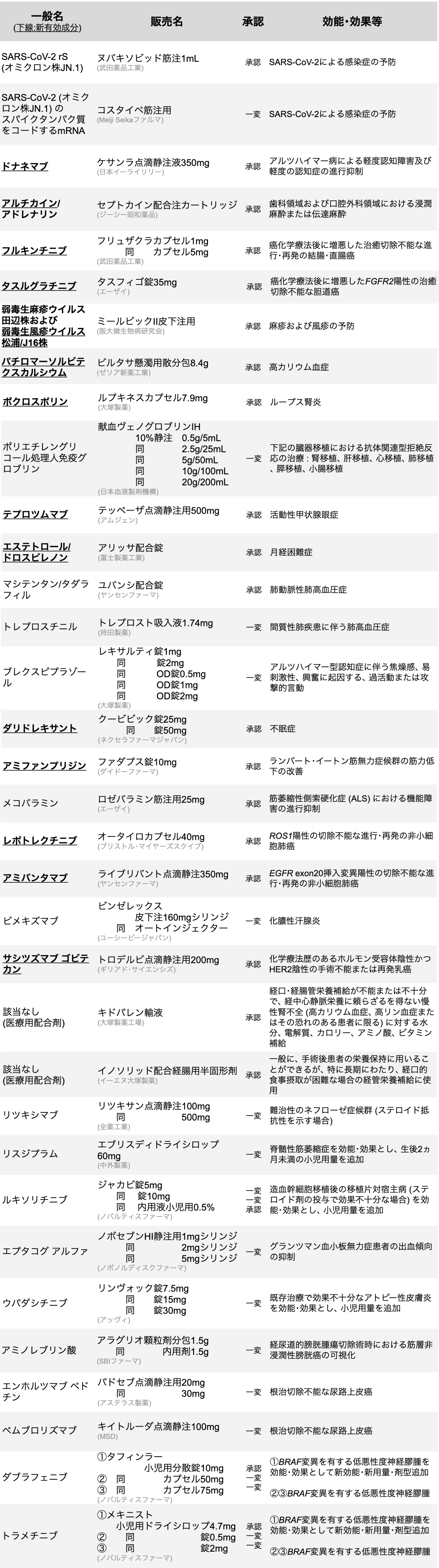
医薬品医療機器総合機構 (PMDA) は、 2024年9月に34種類の医薬品が厚生労働省から承認を受けたと発表した。 (うち新規有効成分は14剤)
アミノレブリン酸
アミノレブリン酸 (商品名アラグリオ®️) は、 経尿道的膀胱腫瘍切除術 (TURBT) 時に筋層非浸潤性膀胱癌を可視化する光線力学診断用薬。
国内第Ⅲ相試験SPP2C102に基づく今回の一部変更承認により、 用法が 「膀胱鏡挿入2~8時間前に、 水に溶解して経口投与」 へと変更された。 これまでに比べ、 同薬の術前投与タイミングが柔軟になったことから、 利便性の向上が期待される。
エンホルツマブ ベドチン
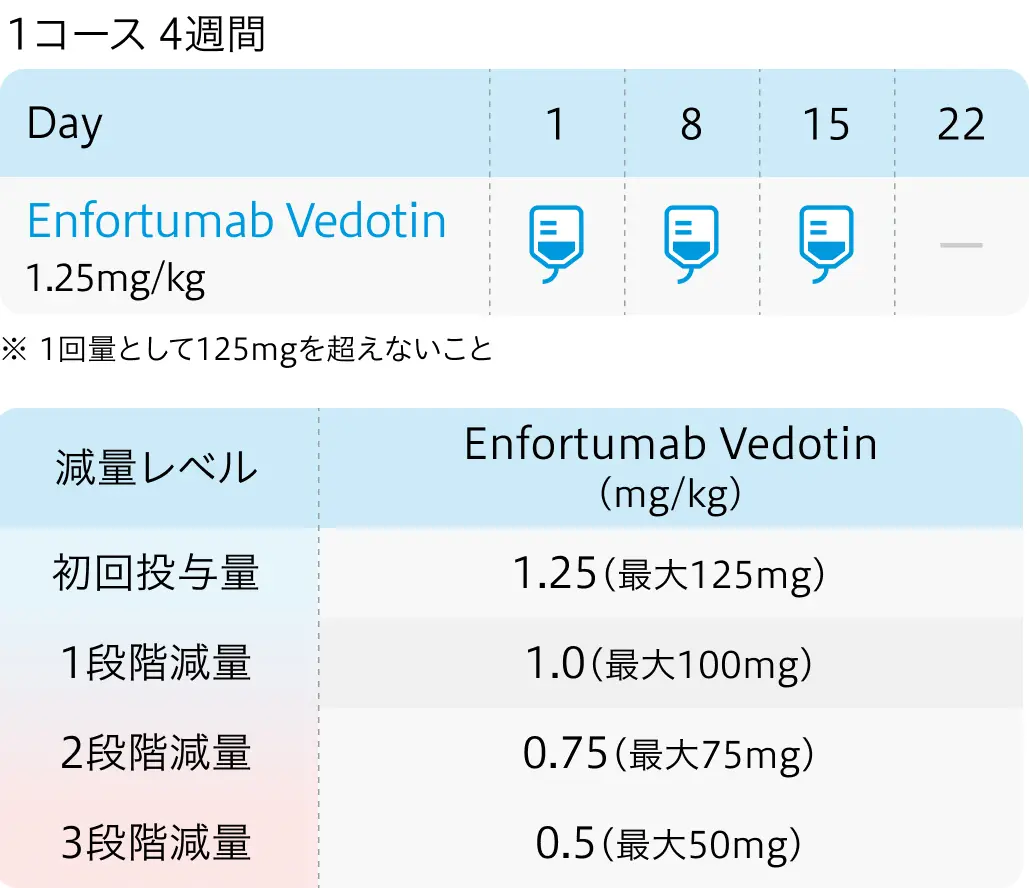
抗Nectin-4標的抗体薬物複合体エンホルツマブ ベドチン (商品名パドセブ®️) は、 根治切除不能な尿路上皮癌に対する1次治療として、 抗PD-1抗体ペムブロリズマブとの併用療法について一部変更承認された。 同併用療法は、 根治切除不能な尿路上皮癌に対する1次標準治療である 「プラチナ白金製剤を含む化学療法」 に代わる、 日本で最初の治療選択肢となる。
今回の承認は、 未治療の局所進行/転移性尿路上皮癌を対象に、 同併用療法の有効性と安全性を評価した第III相無作為化比較試験EV-302/KEYNOTE-A39の結果に基づく。
ペムブロリズマブ
ペムブロリズマブ (商品名キイトルーダ®️) は2017年2月15日に国内で販売を開始した抗PD-1抗体。 今回は上記の通り、 根治切除不能な尿路上皮癌に対する1次治療として、 エンホルツマブ ベドチンとの併用療法について一部変更承認された。
関連コンテンツ
ESMO 2023 Thomas Powles氏
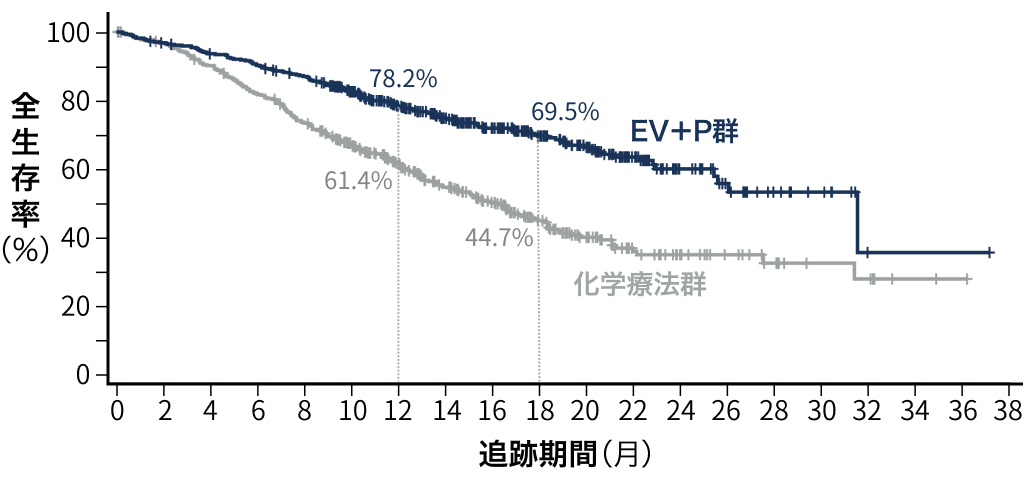
未治療la/mUCへのEV+PはQOL・疼痛を悪化せずPFS・OSを改善
注目の関連コンテンツまとめ
エンホルツマブ ベドチン (パドセブ®︎) | 膀胱癌 > 三次治療以降
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。