Beyond the Evidence
2年前
【解説】大腸癌に対するVEGFR阻害薬フルキンチニブが国内承認
2024年9月24日、 VEGFR1/2/3に対する選択的経口チロシンキナーゼ阻害薬フルキンチニブ (商品名フリュザクラ) が、 「がん化学療法後に増悪した治癒切除不能な進行・再発の結腸・直腸癌」 を適応として国内承認されました。 そこで、「Beyond the Evidence」 シリーズで今春紹介した国立がん研究センター中央病院・廣瀬俊晴氏による解説をあらためてご紹介します。
Clinical Question
大腸癌におけるフルキンチニブの有効性は?
*以下は、2024年4月24日に配信した内容です
専門医の解説 「私はこう考える」

FRESCO試験、 FRESCO-2試験の結果から、遠隔転移再発大腸癌に対し、 3次治療以降でフルキンチニブの有効性が報告されている。 既に米食品医薬品局 (FDA) において承認され、 現在本邦でも承認申請中である。 現状での他の3次治療との直接比較の試験はなく、 実臨床に登場した場合には使い分けや使用順序などの検討課題も多いが、 期待される薬剤である。
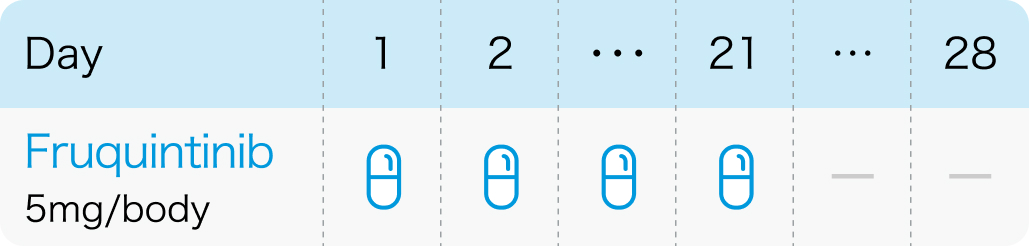
フルキンチニブの概要
VEGFR1/2/3を選択的に阻害する経口薬
フルキンチニブは、 主に血管内皮増殖因子受容体 (VEGFR) に選択性を高くしたチロシンキナーゼ阻害薬 (TKI) である。 一部の補助的な阻害作用として線維芽細胞増殖因子 (FGFR1) や血小板由来増殖因子受容体 (PDGFR)、 RETなどにも作用を示すとされる。
米国、中国ではすでに承認済み
後述する臨床試験の結果から、 2018年に中国で国家薬品監督管理局において、 2023年11月に米食品医薬品局 (FDA) において、 再発・転移性大腸癌に対して承認されている。
※追記 : 本邦でも2024年9月24日に「がん化学療法後に増悪した治癒切除不能な進行・再発の結腸・直腸癌」 を対象として承認された

臨床試験成績
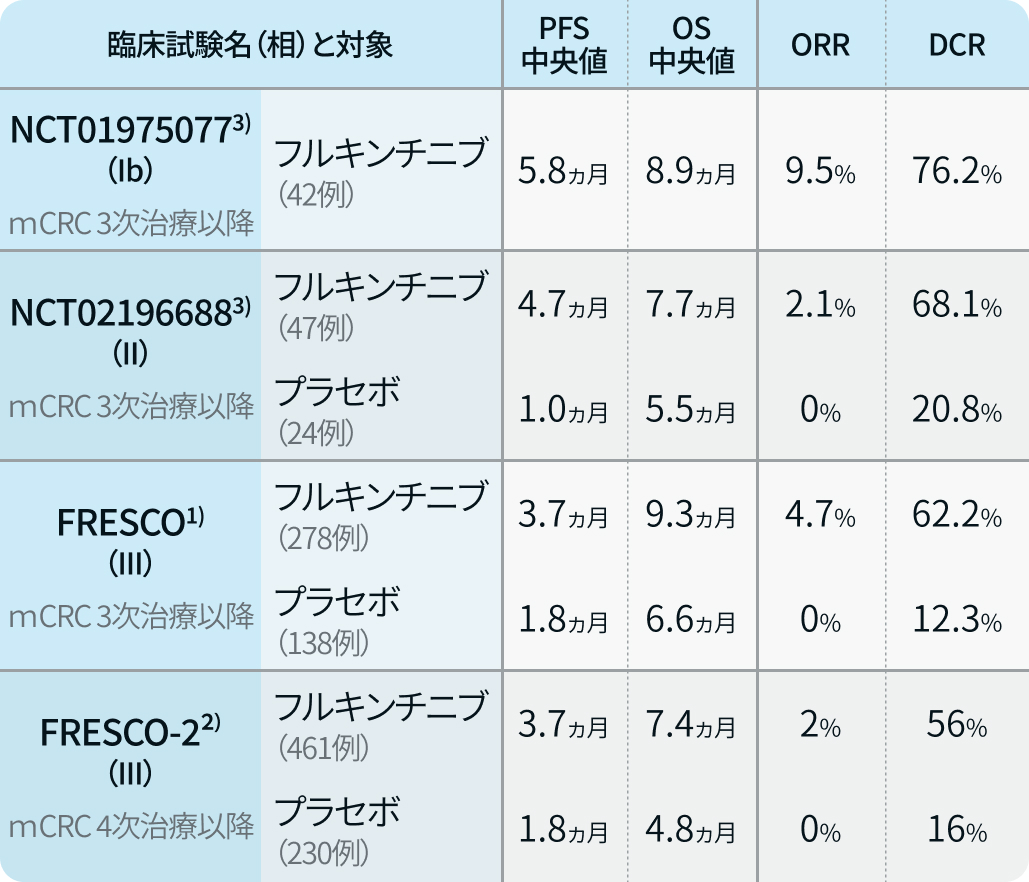
ORR : objective response rate、 DCR : disease control rate、 PFS : progression free survival、 OS : overall survival
筆者提供資料を基に編集部作図
FRESCO試験 >>原著論文を読む
FRESCO試験¹⁾は3次治療以降の切除不能転移性大腸癌を対象として、 中国で実施された第Ⅲ相試験であり、 フルキンチニブとプラセボの2群に2 : 1に無作為化された。 中国の28施設、 416人が無作為化され、 フルキンチニブ群278例、 プラセボ群138例に割り付けられた。
有効性結果|mOS 9.3ヵ月、 mPFS 3.7ヵ月
全生存期間(OS)中央値はフルキンチニブ群とプラセボ群で9.3ヵ月 vs 6.6ヵ月、 HR 0.65 (95%CI 0.51-0.83、 p<0.001)とフルキンチニブ群で有意に良好な結果であり、 主要評価項目を達成していた。 無増悪生存期間 (PFS) 中央値においても3.7ヵ月 vs 1.8ヵ月、 HR 0.26 (同0.21-0.34、 p<0.001) とフルキンチニブ群で良好な結果であり、 奏効割合 (ORR) が4.7% vs 0%、 病勢制御割合 (DCR) に関しても62.2% vs 12.3%とフルキンチニブ群で良好な結果であった。
安全性結果|高血圧、 手足症候群、 蛋白尿など
毒性に関してはフルキンチニブ群においてGrade 3以上の高血圧が21.2%、 手足症候群が10.8%、 蛋白尿が3.2%であった。
FRESCO-2試験 >>原著論文を読む
FRESCO-2試験²⁾はフッ化ピリミジン、 オキサリプラチン、 イリノテカン、 トリフルリジン/チピラシルまたはレゴラフェニブ (もしくは両方) の治療を受けた4次治療以降の切除不能転移性大腸癌を対象として行われた国際共同第Ⅲ相試験であり、 フルキンチニブとプラセボの2群に2 : 1に無作為化された。 691例が無作為化され、 フルキンチニブ群461例、 プラセボ群230例に割り付けられた。
有効性結果|mOS 7.4ヵ月、 mPFS 3.7ヵ月
OS中央値はフルキンチニブ群とプラセボ群で7.4ヵ月 vs 4.8ヵ月、 HR 0.66 (95%CI 0.55-0.80、 p<0.0001) とフルキンチニブ群で有意に良好な結果であった。
PFS中央値においても3.7ヵ月 vs 1.8ヵ月、 HR 0.32 (同0.27-0.39、 p<0.0001) とフルキンチニブ群で良好な結果であり、 DCRに関しても55.5% vs 16.1%と同様に良好な結果であった。
サブグループ解析においても、 前治療歴 (トリフルリジン/チピラシルもしくはレゴラフェニブ)、 RAS遺伝子変異の有無、 一次治療からの期間などを含め、 ほぼすべてのサブグループにおいて、 フルキンチニブ群はプラセボ群と比較してOSとPFSが良好な結果となっていた。
安全性結果|高血圧、 倦怠感など
フルキンチニブ群とプラセボ群において頻度が高かったGrade 3以上の治療関連有害事象は、 高血圧(14% vs 1%)、 倦怠感(8% vs 4%)、 食欲低下(2% vs 1%)、 下痢(4% vs 0%)であった。
臨床試験から見えてきた課題
3次治療における薬剤選択
FRESCO試験では3次治療としてフルキンチニブが投与されているが、 3次治療においてフルキンチニブ、 トリフルリジン/チピラシル (+ベバシズマブ)、 レゴラフェニブのいずれを使用するのがよいか直接比較した試験はなく、 今後検討が必要である。
4次治療における有効性
FRESCO-2試験の結果から、 フルキンチニブはトリフルリジン/チピラシルもしくはレゴラフェニブを使用した後、 4次治療でも良好な有効性を示していた。
FRESCO-2試験においては、 フルキンチニブ群の約96%が抗VEGF抗体の投与を受けており、 フルキンチニブが前治療の血管新生阻害薬の有無に関わらず有効であることが示されている。
一方でこの試験の対象となったのはトリフルリジン/チピラシル単剤もしくはレゴラフェニブ単剤での病勢進行となった患者で、 プラセボ群との比較試験であった。 現状での3次治療においてはSUNLIGHT試験の結果からトリフルリジン/チピラシル+ベバシズマブ療法が標準治療として確立しており、 この対象の後に病勢進行となった場合のエビデンスはまだない。
毒性プロファイル
毒性プロファイルに関しては、 フルキンチニブでは従来のTKIと同様に高血圧や蛋白尿、 手足症候群の副作用が報告されていた¹⁾⁻³⁾。 フルキンチニブによる治療を受けた患者の休薬は47%であり、 減量は24%であった²⁾。
これは同様のTKIであるレゴラフェニブと比較すると休薬と減量ともに少ない結果であり、 フルキンチニブは比較的負担なく使える可能性が示唆される。 一方でトリフルリジン/チピラシルに関しては骨髄抑制が主な副作用であり、 この部分が使い分けの目安になると考える。
薬剤の使用順序
使用順序に関しては、 レゴラフェニブを使用した後にフルキンチニブを使用した方が生存期間が良かったとの報告もある⁴⁾が、 まだエビデンスとしては不十分であり、 こちらも今後の検討課題である。
最後に
フルキンチニブは本邦で承認申請中であり、 今後近いうちに保険承認されることが期待される。 実臨床での使い分けや治療順の戦略など課題はあるものの、 長らく登場していなかった大腸癌に対する新規薬剤であり、 注目される薬剤である。
※追記 : 本邦でも2024年9月24日に「がん化学療法後に増悪した治癒切除不能な進行・再発の結腸・直腸癌」 を対象として承認、 2024年11月22日に薬価収載、販売開始となった
出典
1) Effect of Fruquintinib vs Placebo on Overall Survival in Patients With Previously Treated Metastatic Colorectal Cancer: The FRESCO Randomized Clinical Trial. JAMA. 2018 Jun 26;319(24):2486-2496. PMID: 29946728
2) Fruquintinib versus placebo in patients with refractory metastatic colorectal cancer (FRESCO-2): an international, multicentre, randomised, double-blind, phase 3 study. Lancet. 2023 Jul 1;402(10395):41-53. PMID: 37331369
3) Safety and efficacy of fruquintinib in patients with previously treated metastatic colorectal cancer: a phase Ib study and a randomized double-blind phase II study. J Hematol Oncol. 2017 Jan 19;10(1):22. PMID: 28103904
4) Comparison of the efficacy and safety of fruquintinib and regorafenib in the treatment of metastatic colorectal cancer: A real-world study. Front Oncol. 2023 Mar 3:13:1097911. PMID: 36937443
関連コンテンツ
9月の承認情報まとめ
第20回日本臨床腫瘍学会レポート
Lancet. 2023 Jul 1;402(10395):41-53.
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。